中华医学会
地址: 中国北京东四西大街42号
邮编: 100710
判断新生儿坏死性小肠结肠炎手术指征的列线图模型建立与验证
摘要
目的
探讨新生儿坏死性小肠结肠炎(necrotizing enterocolitis,NEC)患儿需手术治疗的独立危险因素,并构建识别需外科手术的NEC患儿的列线图模型。
方法
回顾性选择2020年1月至2023年12月郑州大学第三附属医院新生儿外科收治的NEC患儿为研究对象,前2年病例纳入训练集,后1年病例纳入验证集。根据患儿是否手术治疗,训练集和验证集再分为手术组和非手术组,比较两组患儿一般资料、腹部查体情况、实验室检查结果、腹部影像学及超声结果,利用多因素logistic回归寻找NEC患儿需手术治疗的独立危险因素,根据这些因素构建列线图模型并验证。
结果
共纳入923例NEC患儿,其中训练集746例,验证集177例。对临床资料进行logistic回归分析,结果显示出生体重、腹胀加重、腹部压痛、腹肌紧张、C反应蛋白升高、血钠降低、腹部超声发现门静脉积气、腹部超声发现腹腔积液8个因素是NEC需行手术治疗的独立危险因素,构建判断NEC手术指征的列线图模型。其中训练集受试者工作特征曲线下面积(area under the curve,AUC)为0.976(95% CI 0.959~0.993),验证集AUC为0.964(95% CI 0.935~0.993)。对模型进行Hosmer-Lemeshow拟合优度检验,结果提示模型拟合良好。根据得到的模型,对所有手术病例进行赋分并查阅手术记录,以5分为一个区间进行分析,分值为>25~30分、>30~35分、>35~40分的患儿处于最佳手术时机的例数较多。
结论
出生体重、腹胀加重、腹部压痛、腹肌紧张、C反应蛋白升高、血钠降低、超声门静脉积气、超声腹腔积液是提示NEC患儿需外科手术的独立危险因素,构建的列线图模型展现出了良好的价值,可用于辅助临床判断NEC患儿是否需要手术。
新生儿坏死性小肠结肠炎(neonatal necrotizing enterocolitis,NEC)是新生儿期特有的消化道疾病[1] 。在NEC患儿的外科治疗中,判断手术时机非常重要,这依赖于临床医生的经验,但可能会判断失误,延误手术时机,导致患儿病情进展,预后不良。有些患儿经内科保守治疗后病情即可好转,但若没能很好地将这些可保守治疗的内科NEC患儿与需手术治疗的外科NEC患儿区分开来,会对这些患儿造成不必要的损伤,因此,掌握NEC的外科手术指征至关重要。目前研究发现提示患儿需手术的指标很多,如C反应蛋白(C-reactive protein,CRP)、降钙素原(procalcitonin,PCT)、超声发现门静脉积气、使用有创呼吸机等等[2,3] ,但较少有研究将其统一量化,因此实际应用起来相对复杂。如果能对这些指标进行量化,将有利于新生儿科及儿外科医生更好地把握手术时机。本研究旨在构建一个更加直观的辅助临床医生决策的列线图模型。
对象和方法
一 研究对象
选择2020年1月至2023年12月郑州大学第三附属医院新生儿外科收治的NEC新生儿进行回顾性分析,其中2020—2022年收治的患儿纳入训练集,2023年收治的患儿纳入验证集。入选标准:经手术证实为NEC或诊断Bell分期Ⅱ期以上的NEC患儿。排除标准:(1)合并复杂先天性心脏病等严重疾病或先天性巨结肠等其他消化道畸形的患儿;(2)患儿因病情危重无法耐受手术治疗;(3)家属拒绝进一步治疗或未在我院行手术治疗。本研究通过我院医学伦理委员会审批(2022-124-01)。
二 研究方法
1.资料收集:通过查阅电子病历收集患儿以下资料:(1)一般情况:性别、胎龄、出生体重、分娩方式、喂养方式。(2)NEC病程中出现的症状:腹胀、便血、呕吐等消化道表现、是否有腹胀加重表现(指采取禁食水、胃肠减压等内科保守治疗后腹胀仍加重)。(3)体格检查:腹部压痛、腹肌紧张、腹部包块、腹壁红斑、肠鸣音减弱。(4)实验室检查:CRP升高、白细胞变化、血小板变化、PCT升高、血钠降低、血培养结果;其中手术组取术前最后一次检查结果,非手术组取NEC病程中偏离正常值最大的结果。(5)影像学表现:肠管积气、肠间隙增宽、肠壁增厚、肠壁积气或可疑积气、门静脉积气、气腹、腹腔积液等。
2.NEC手术指征[4] :(1)发生肠穿孔;(2)经内科保守治疗无效或病情持续加重。手术患儿均由新生儿科及儿外科副高级以上医师评估。
三 统计学方法
应用SPSS 26.0统计软件进行数据分析。正态分布的计量资料以均值±标准差表示,组间比较采用 t检验;非正态分布的计量资料以 M( Q 1, Q 3)表示,组间比较采用Mann-Whitney U检验;计数资料以例(%)表示,组间比较采用 χ 2检验。采用单因素logistic回归进行单因素分析,为尽可能纳入有意义的指标,单因素分析时以 P<0.1为差异有统计学意义;采用二元logistic回归进行多因素分析,以 P<0.05为差异有统计学意义。
使用Stata 15.0统计软件进行Nomogram模型的建立及验证,绘制模型的受试者工作特征(receiver operator characteristic,ROC)曲线,计算其曲线下面积(area under the curve,AUC)。利用Hosmer-Lemeshow拟合优度检验评价模型的准确性,校准曲线评估模型准确度,利用临床决策曲线评价模型的实用性。
结 果
一 一般结果
研究期间共收治NEC新生儿1 183例,其中未明确诊断8例,合并其他严重疾病或消化道畸形193例,家属拒绝进一步治疗或未在我院行手术治疗59例,共纳入923例,其中手术患儿共220例(23.8%)。
训练集纳入746例,手术组176例,非手术组570例;验证集纳入177例,手术组44例,非手术组133例。
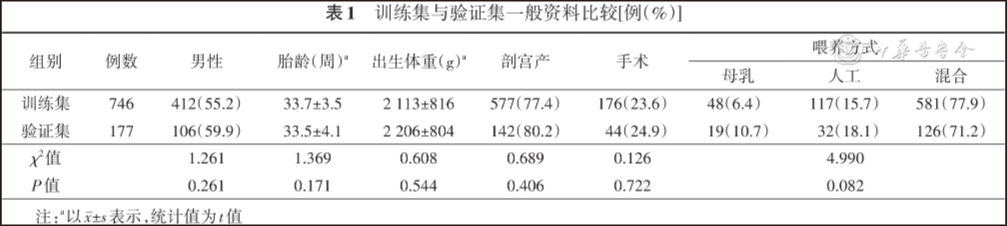
二 训练集和验证集一般资料比较
训练集和验证集一般资料比较差异无统计学意义( P>0.05),见表1 。
三 训练集手术组与非手术组临床资料单因素分析
训练集手术组患儿与非手术组患儿单因素logistic回归分析显示,两组患儿一般情况(胎龄、分娩方式、出生体重、生后喂养方式)、体格检查(腹胀、腹胀加重、便血、腹部压痛、腹肌紧张、腹壁红斑、肠鸣音减弱)、实验室检查(白细胞降低、CRP升高、PCT升高、血小板、血钠、血培养)、影像学检查(肠壁增厚、肠壁积气、门静脉积气、气腹、腹腔积液)等方面存在差异,差异有统计学意义(P<0.05),见表2,3,4,5。
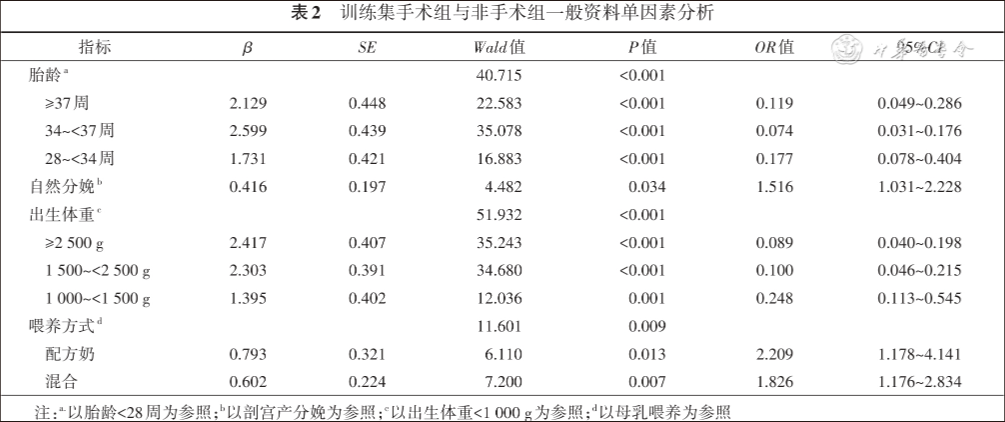
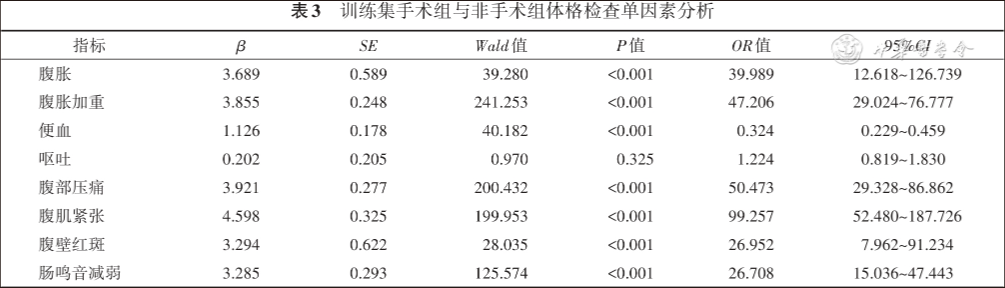
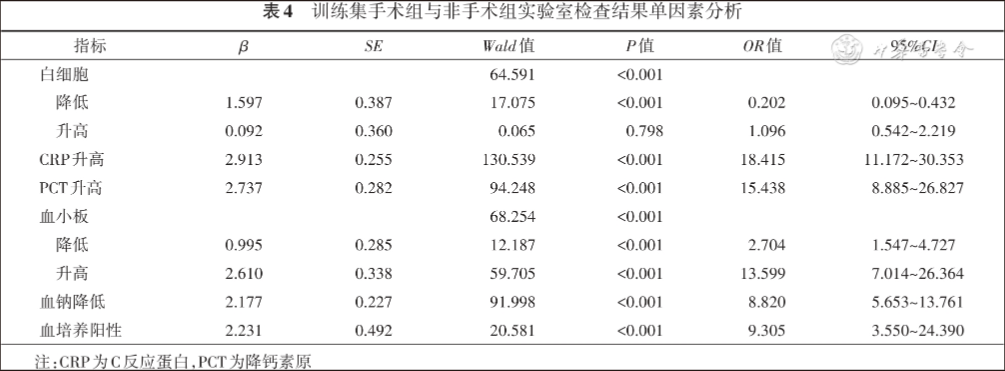
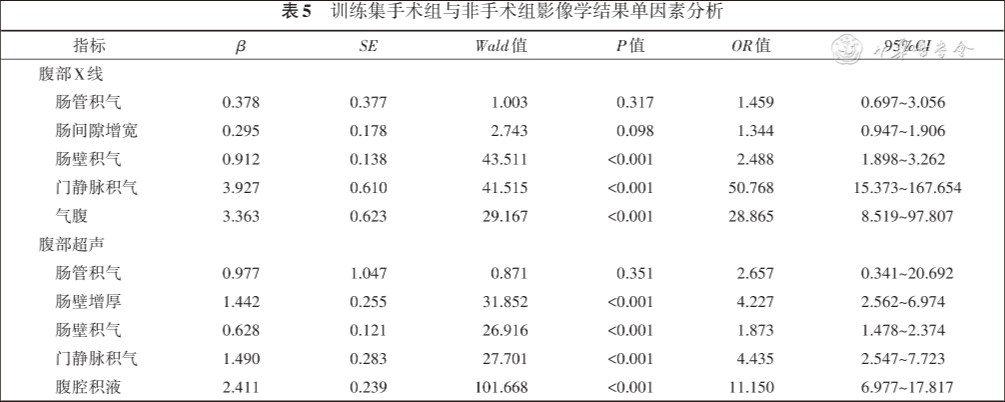
四 多因素logistic回归分析
将单因素回归分析中有统计学意义的变量纳入多因素logistic回归模型中。结果显示,出生体重低、腹胀加重、腹部压痛、腹肌紧张、CRP升高、血钠降低、腹部超声门静脉积气、腹部超声提示透声差的腹腔积液8个因素是NEC患儿需行手术治疗的独立危险因素,见表6。
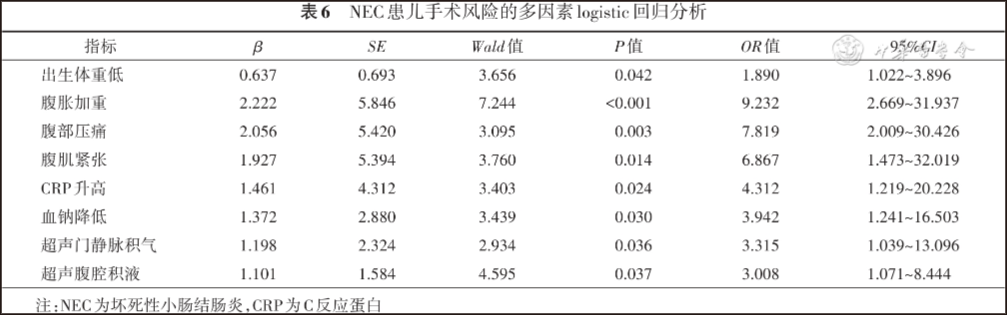
五 列线图模型构建
应用Stata 15.0软件,根据多因素logistic回归分析结果,纳入有统计学意义的8个变量并根据其 OR值进行赋分,构建识别需手术的NEC患儿的列线图模型,见 图1 ,其中出生体重>2 500 g为2.5分、1 500~2 499 g为5.0分、1 000~1 499 g为7.5分、<1 000 g为10.0分;腹胀加重为8.8分,腹部压痛为8.1分,腹肌紧张为7.6分,CRP升高为5.8分,血钠降低为5.3分,超声门静脉积气为4.7分,超声提示腹腔内透声佳的积液为4.3分,透声差的积液为8.6分。假如一位诊断为NEC的患儿出生体重在1 500~2 499 g之间,有腹部压痛、腹肌紧张、CRP升高,超声提示腹腔内有透声佳的积液,那么这位患儿总分值为30.8分,手术风险约为70%。
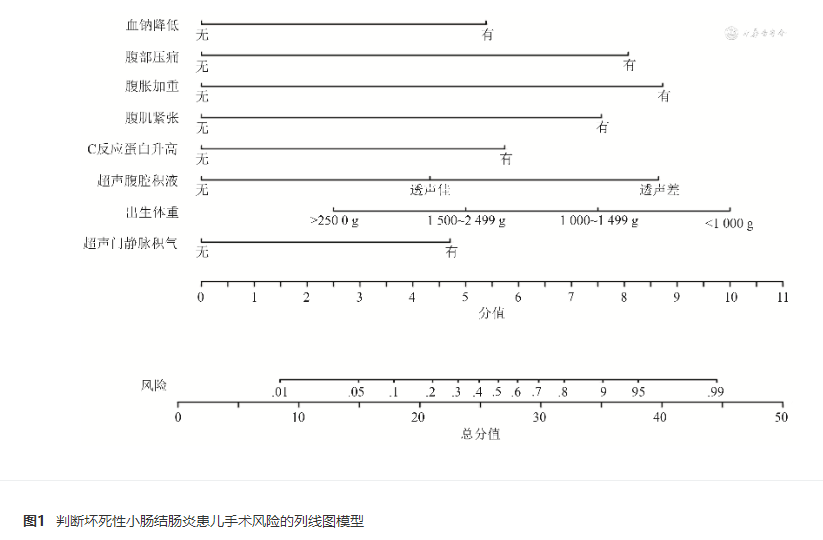
六 模型的评价与验证
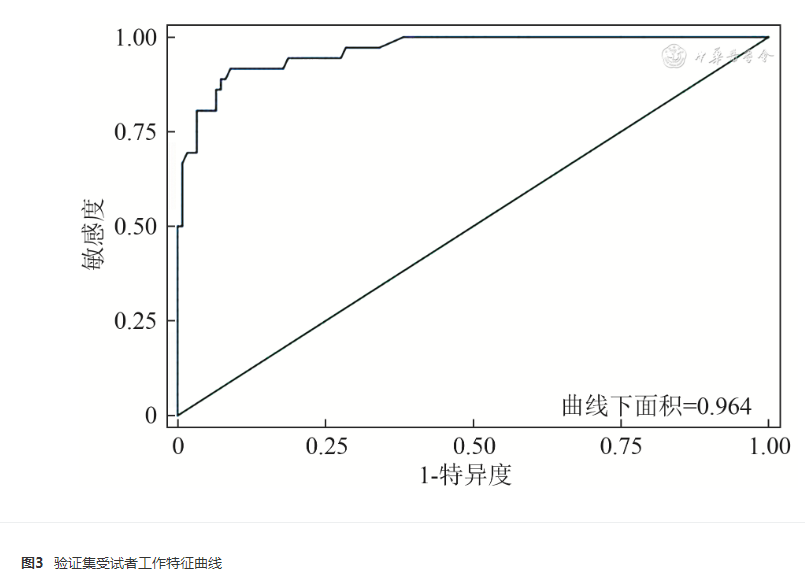
对训练集及验证集分别绘制ROC曲线,计算AUC,结果显示,训练集AUC为0.976(95% CI 0.959~0.993),验证集AUC为0.964(95% CI 0.935~0.993),见图2、3。
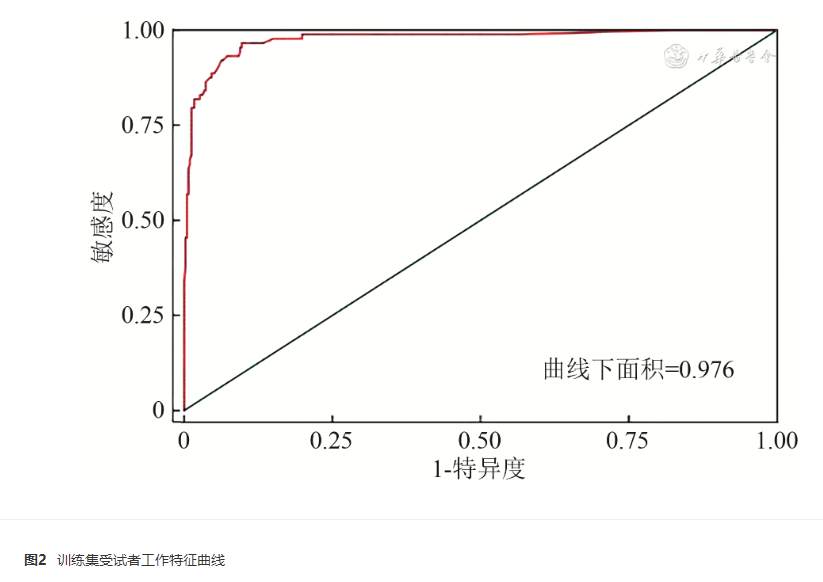
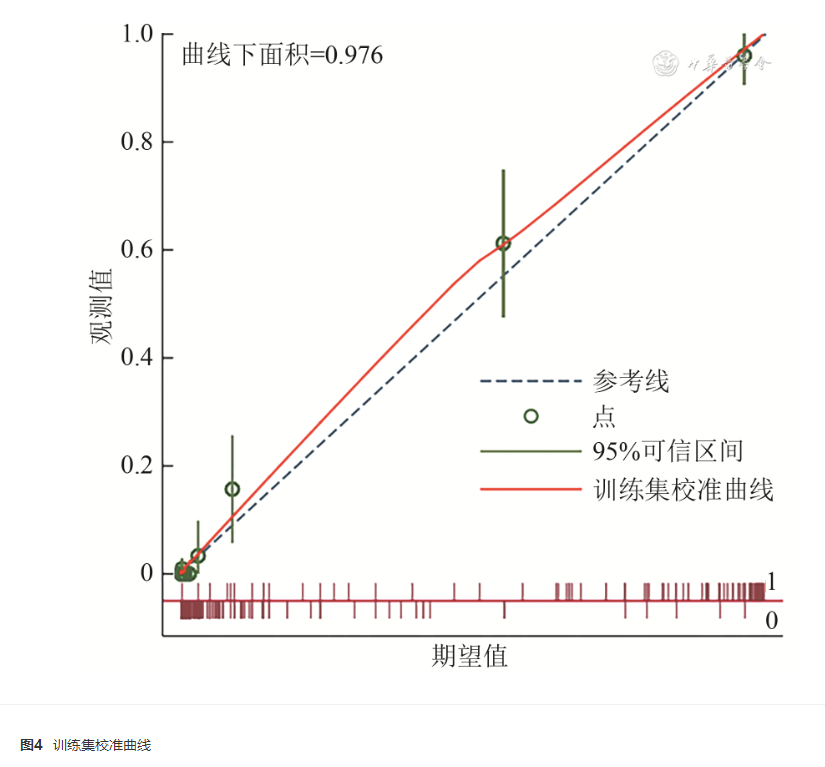
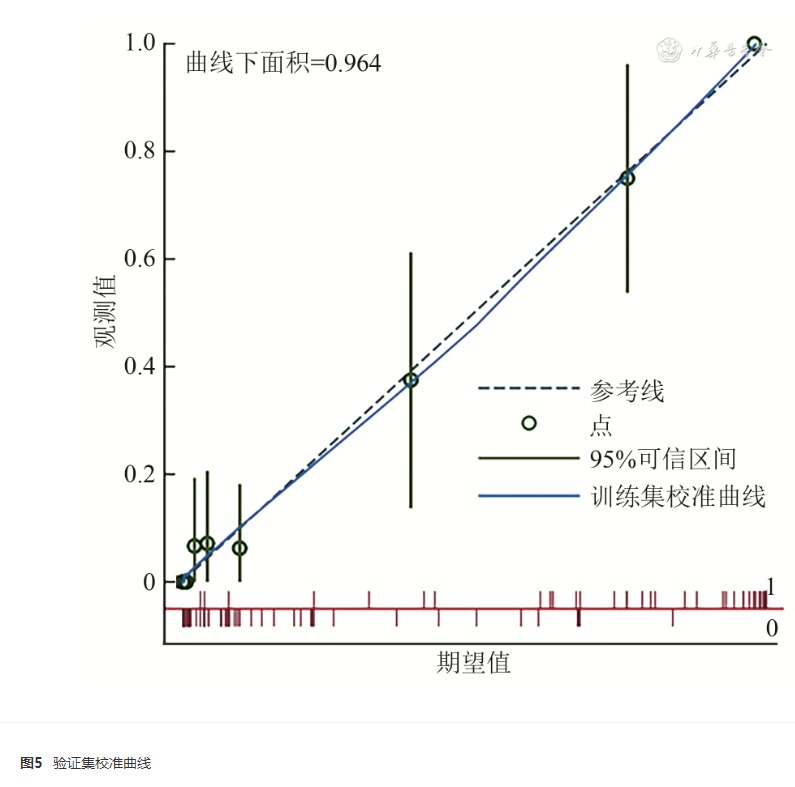
对模型进行Hosmer-Lemeshow拟合优度检验,得到 χ 2 =6.08,自由度=9, P=0.732, P>0.05提示模型拟合良好,并分别绘制校准曲线,结果显示曲线拟合良好,见图4、5。
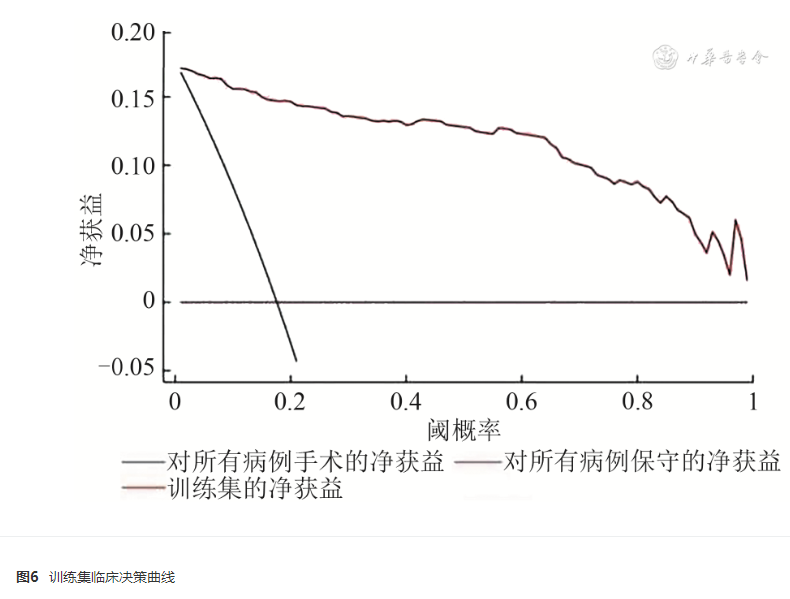
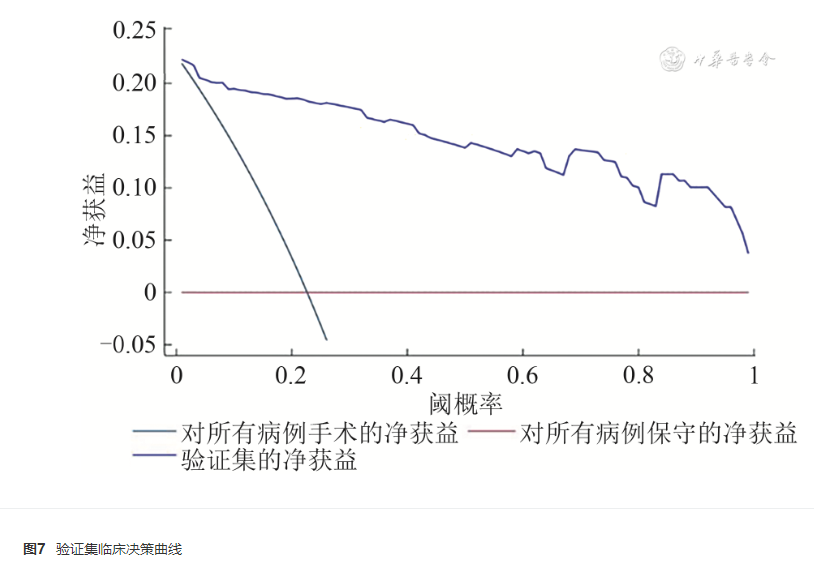
以风险阈值为横坐标,以净获益为纵坐标,对训练集与验证集分别绘制临床决策曲线(图6、7),图中的深棕色线(即图中纵坐标为0的横线)代表对所有患儿均不进行手术干预,净获益为0;蓝色斜线表示对所有患儿均手术干预,净获益为该线的斜率,即负值。风险阈值取值在蓝色斜线和红线之间时(0.18~1),患儿可获得净获益。这表明利用该列线图模型对NEC患儿手术风险进行判断,进而对患儿进行手术干预,可以使患儿获益。
七 评分分析
依据本研究得出的列线图,将本研究中的所有病例纳入并评分。查阅所有手术组病例的手术记录,以5分为一个区间对评分进行分析,当手术记录中描述患儿肠管发生片状或节段性坏死而未发生穿孔时,认为该患儿处于最佳手术时机[4]。将所有患儿汇总得到以下结果,见表7。
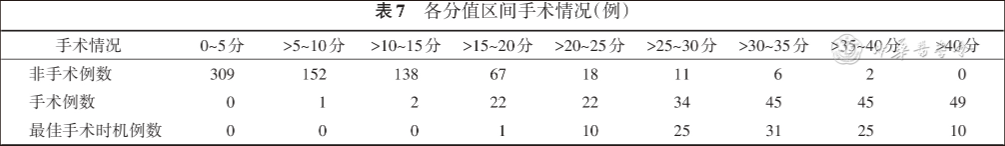
通过分析以上表格发现,分值为>25~30分、>30~35分、>35~40分的患儿处于最佳手术时机的例数较多。
讨 论
NEC是新生儿时期一种常见的严重消化道疾病,并不都是感染导致。新生儿重症监护室患儿NEC发生率为2%~5%,随着早产儿救治率的提高,发生率呈上升趋势[5,6]。NEC病死率较高,在超低出生体重儿中可达30%~50.9%[7]。虽然多数NEC患儿经内科保守治疗可好转,但仍有20%~40%的患儿需手术治疗[8],本研究中手术患儿比例约24%,与文献报道一致。有些NEC患儿病情进展很快,手术时已发生肠穿孔或大面积肠坏死,导致患儿预后不佳[9]。而对可内科保守治疗的患儿不恰当地进行手术干预反而会增加不必要的损害。因此,如何判断NEC患儿是否需要进行手术便显得尤为重要,目前关于提示需行手术的危险因素相关的研究很多,但较少有研究将这些指标进行统一量化,本研究旨在将这些指标量化,从而构建一个辅助临床医生决策的列线图模型。
本研究发现腹胀加重、腹部压痛和腹肌紧张是NEC患儿需行手术治疗的独立危险因素,这与梁木和宋晓峰[10]的研究一致。当体格检查出现腹部触痛和腹肌紧张时,往往肠道炎症较重,可能出现了腹膜炎,提示患儿需要行手术治疗的可能性增加,当肠道炎症进一步加重,发生肠坏死时,腹壁可能会发生色泽改变,腹壁出现红斑[11],这些都反映了病情的严重程度,可以辅助判断是否需要行手术治疗,不过目前现有的NEC诊断评分系统里,很少有将临床表现这些指标量化并纳入的[12,13,14]。
本研究通过多因素分析发现CRP升高是影响手术风险的独立危险因素。CRP升高与全身炎症反应有关,Yu等[15]认为,全身炎症反应在一定程度上反映肠道炎症程度,并能用于辅助诊断外科NEC。同样,CRP作为一种急性时相蛋白,也会在全身炎症反应时升高,Mohd等[16]发现,CRP与白蛋白之比也可以用于判断手术风险,当NEC第2天的CRP/白蛋白≥3时,患儿手术风险更高。既往研究已经证明,CRP是判断手术风险的一项重要指标[10,15],在实际临床应用中也经常被临床医生参考。不过,关于CRP升高在手术风险的判断中占有的权重,目前研究较少,本研究纳入了CRP升高这一指标,并通过一系列的统计学分析后最终赋分5.8分,这一结果可为临床医生提供一定的参考。
超声检查时发现的门静脉积气和透声差的腹腔积液也是提示需行手术治疗的独立危险因素,被纳入了模型,分值分别为4.7分、8.6分。Lazow等[17]的研究认为,肠壁积气通过肠系膜血管及淋巴管进入门静脉,便会出现门静脉积气[18,19],同时这也是NEC特有的征象,可以在一定程度上反映肠道炎症的程度。透声差的腹腔积液提示可能发生了腹腔内感染或肠穿孔,这反映了肠坏死的程度,且分值也较高,这与实际临床经验也相符。
在构建完成列线图模型后,本研究对纳入的所有患儿进行了评分及分析。以5分为一个区间,0~20分的患儿大多行保守治疗,而行手术治疗的患儿也大多未发生肠管坏死,并非在最佳手术时机。>20~25分的患儿手术治疗和保守治疗的例数相近(22比18),此时应是最引起争议的情况,通过查阅此区间的手术记录,发现有10例患儿的肠管发生片状坏死或节段性坏死,处于最佳手术时机,占比约45%,然而仍有9例仅有肠管水肿,未发生坏死穿孔,3例仅有极小的点状坏死。当总分值为>25~30分时,手术病例明显多于保守病例,比例大约为3∶1,查阅此区间患儿的手术记录,发现有25例患儿的肠管已经发生明确的片状或节段性坏死,未发生穿孔或将近穿孔,处于最佳手术时机,占比约74%。此区间的最佳手术病例占比最高,因此,本研究认为在分值达到>25~30分时,应引起临床医师足够的警惕,此时手术风险较高,且患儿处于最佳手术时机的可能性也较大。此区间有32例患儿处于Bell Ⅱb级,与张志波[20]认为的最佳手术时机一致。当总分值在30分以上时,手术治疗比例与保守治疗比例达17∶1,绝大部分患儿需要手术治疗,此区间有55例发生了穿孔,15例发生了肠管大面积的坏死甚至全肠坏死,穿孔率接近40%,此时临床医生应高度警惕,患儿的病情可能较为严重,手术风险很高。
本研究的模型纳入指标与修正Bell分级类似[21],另外还纳入了患儿的出生体重、腹部超声等指标,本研究的模型对各影响因素进行了量化,不同的分值代表了不同的危险程度,相比于修正Bell分级的6个级别,这是本研究的不同之处。不过,本模型也有许多待进一步完善的地方,如腹胀加重、腹部触痛这些指标存在主观因素,后续研究中需纳入如腹围等更客观的数据来使这一结果更加准确。同时,模型也存在预测不精准问题,例如有部分患儿虽然评分很低但发生了肠穿孔甚至大面积肠坏死,这可能是由于评分主要取决于术前的检查结果,而某些患儿病情变化快,术前结果可能不能及时反映病情变化,后续需要更深入的研究来对模型进一步完善并且验证。
引用本文: 袁洋,黄华,陈玄玄,等. 判断新生儿坏死性小肠结肠炎手术指征的列线图模型建立与验证[J]. 中华新生儿科杂志(中英文),2025,40(05):264-271.DOI:10.3760/cma.j.cn101451-20240913-00325.
