中华医学会
地址: 中国北京东四西大街42号
邮编: 100710
妊娠合并胸主动脉疾病诊断与治疗专家共识(2026)
选自:中华妇产科杂志2026年3月第61卷第3期
作者:中国医师协会心血管外科医师分会大血管外科专业委员会、中国人体健康科技促进会 心脑血管危重症产科专业委员会、北京医学会心脏外科学分会
通 信 作 者:朱 俊 明,首 都 医 科 大 学 附 属 北 京 安 贞 医 院 主 动 脉 外 科 中 心,Email:anzhenzjm@163.com;张军,首都医科大学附属北京安贞医院妇产科 心血管重症妇产医学中心,Email:drzhangj@outlook.com
引用本文:中国医师协会心血管外科医师分会大血管外科专业委员会,中国人体健康科技促进会心脑血管危重症产科专业委员会,北京医学会心脏外科学分会. 妊娠合并胸主动脉疾病诊断与治疗专家共识(2026)[J]. 中华妇产科杂志,2026,61(03):177-189.DOI:10.3760/cma.j.cn112141-20251012-00478
摘要
妊娠合并胸主动脉疾病是严重威胁母儿生命的危重症,但我国尚缺乏统一的诊疗规范。为填补此领域的空白,中国医师协会心血管外科医师分会大血管外科专业委员会、中国人体健康科技促进会心脑血管危重症产科专业委员会和北京医学会心脏外科学分会结合我国国情和国内外相关领域研究进展,联合制订《妊娠合并胸主动脉疾病诊断与治疗专家共识(2026)》。本共识对当前可获得的国内外最佳证据质量及推荐意见进行分级,综合衡量安全性、有效性、可行性、可及性和成本效益等因素后形成推荐意见。系统阐述了妊娠合并胸主动脉疾病医疗活动中涉及的诊断与评估、治疗与处理原则和妊娠指导等8个临床问题,形成45条推荐意见,并着重提出精细化手术时机选择、围手术期麻醉与体外循环管理、分娩方式等多学科管理策略,旨在为临床医师提供权威、实用的诊疗指导,以期改善母儿预后。
妊娠合并胸主动脉疾病是主动脉疾病中的特殊类型,主要包括主动脉扩张、主动脉瘤和主动脉夹层(aortic dissection,AD)等。妊娠期生理改变、妊娠期高血压疾病、遗传性结缔组织病等与妊娠期胸主动脉疾病相关,其中,遗传性结缔组织病是发病的主要危险因素 [ 1 , 2 , 3 , 4 ] 。对于所有罹患主动脉疾病的育龄期女性患者,妊娠期和产褥期是发生主动脉疾病的高危时期。由于主动脉瘤早期常无明显临床表现而难以察觉,患者常以AD或相关并发症表现就诊。而妊娠期发生AD将严重威胁孕产妇及胎儿的生命。
根据《2024年我国卫生健康事业发展统计公报》 [ 5 ] 报道,全国孕产妇死亡率较往年显著下降,但是心血管疾病仍是孕产妇非产科死亡的首要原因,威胁母儿健康。妊娠合并胸主动脉疾病起病隐匿、误诊率及致死率高、预后差,目前我国对此类疾病的管理仅基于少数医院多学科团队协作的临床经验,缺乏规范诊疗共识。鉴于此,中国医师协会心血管外科医师分会大血管外科专业委员会、中国人体健康科技促进会心脑血管危重症产科专业委员会和北京医学会心脏外科学分会共同发起,组织此领域专家拟定关键问题,根据最新临床研究结果,参考国际权威性文件,结合我国国情及临床实践,经两轮德尔菲调研和专家讨论,形成共识推荐意见,最终制订《妊娠合并胸主动脉疾病诊断与治疗专家共识(2026)》。内容涉及胸主动脉疾病诊断与评估、治疗与处理原则和妊娠指导等8个临床问题,形成45条推荐意见。见 表1 。

一、妊娠对主动脉的影响
为了满足子宫胎盘循环的需要,妊娠期血流动力学有以下变化:(1)主动脉壁张力增加:妊娠期女性心输出量增加30%~50%,伴随心率加快(增加20%~40%)和每搏输出量增加;妊娠20周前孕妇的外周血管阻力下降,导致血压下降,妊娠20周后血压逐渐升高10%~20%直至分娩。因此,孕妇的循环容量负荷增加,在妊娠32~34周达到高峰,导致主动脉壁张力增加,主动脉直径生理性增宽约5% [ 6 , 7 , 8 ] ,但马方综合征(Marfan syndrome,MFS)孕妇则可能增宽约23% [ 9 ] 。(2)主动脉壁微结构改变:妊娠期雌激素和孕激素水平的变化改变主动脉中膜、内膜的微结构,导致网状纤维断裂、弹性纤维波状结构消失、黏多糖水平降低,从而使主动脉壁对抗血流动力学变化的能力下降 [ 10 , 11 ] ;另有动物实验证明,催产素与妊娠晚期及产后4周内AD的发生显著相关 [ 12 ] 。同时,妊娠期子宫增大压迫髂动脉,导致血流阻力增大。因此,妊娠期主动脉呈现的生理性改变可能增加了孕妇胸主动脉疾病的发生风险 [ 13 ] 。
二、妊娠合并胸主动脉疾病多学科团队
妊娠合并胸主动脉疾病多学科团队应由心外科医师、妇产科医师、麻醉科医师、体外循环(cardiopulmonary bypass,CPB)医师及重症监护医师组成,且都具有管理妊娠合并胸主动脉疾病的专业知识及临床经验。对于有条件的医疗中心,可扩大涉及医学遗传学专家、生殖医学专家、新生儿科专家、护理学专家、心脏病学专家、肺血管病专家,以及其他相关领域专家。根据修订版世界卫生组织(mWHO)妊娠风险分级,建议中危及以上(即≥mWHO风险Ⅱ~Ⅲ级)的育龄期妇女,妊娠前、妊娠期间、分娩前和产褥期应在妊娠合并胸主动脉疾病多学科团队所在区域性中心接受孕前咨询和妊娠期管理 [ 14 ] 。妊娠合并胸主动脉疾病多学科团队应全面评估孕产妇心血管疾病、产科疾病的发生风险和胎儿宫内不良事件的发生风险,制定妊娠期综合管理策略。同时,妊娠合并胸主动脉疾病多学科团队应具备区域性诊疗能力,讨论来自其他医疗中心的危重病例。若患者在不具备多学科团队诊疗条件的医院确诊或可疑妊娠合并胸主动脉疾病,应快速稳定病情,及时转诊至设立有妊娠合并胸主动脉疾病多学科团队的机构进一步诊治。
三、妊娠合并胸主动脉疾病的常见类型
(一)胸主动脉扩张或胸主动脉瘤
主动脉直径增加是多数胸主动脉疾病的早期表现。正常育龄期妇女主动脉根部和升主动脉直径不超过3.5 cm,主动脉扩张超过正常直径的50%者称为主动脉瘤 [ 15 ] 。主动脉扩张或主动脉瘤病变中,以主动脉根部或升主动脉扩张较为常见,如未接受有效监测和干预,可进展为AD或导致主动脉破裂。一项对964例未手术的升主动脉瘤患者长期随访的研究结果显示,升主动脉直径为3.5~3.9 cm时,主动脉不良事件(包括AD、主动脉破裂及其导致的死亡)的年发生率为0.3%,而直径扩张至5.0~5.4 cm和≥5.5 cm的主动脉不良事件的年发生率分别为1.1%和2.5% [ 16 ] 。
(二)AD
1. 定义:AD是由各种原因导致的主动脉内膜、中膜撕裂,主动脉内膜与中膜分离,血液流入,致使主动脉腔被分隔为真腔和假腔。典型的AD可见位于真、假腔之间的分隔或内膜片 [ 17 ] 。
2. 分型与分期:(1)DeBakey分型:根据AD原发破口位置及累及范围分型。Ⅰ型:原发破口位于升主动脉或主动脉弓,夹层累及至降主动脉或主动脉全程。Ⅱ型:原发破口位于升主动脉,夹层累及升主动脉或部分主动脉弓。Ⅲ型:原发破口位于左锁骨下动脉开口远端,夹层局限于胸降主动脉(Ⅲa型)或向下同时累及腹主动脉(Ⅲb型)。(2)Stanford分型:根据夹层累及范围分型。凡是夹层累及升主动脉者为Stanford A型,相当于DeBakey Ⅰ型和Ⅱ型;夹层仅累及胸主动脉、降主动脉及其远端为Stanford B型,相当于DeBakey Ⅲ型 [ 13 ] 。(3)孙氏分型:在Stanford分型基础上提出的细化分型 [ 7 ] ,国内应用较为广泛。Stanford A型根据主动脉根部受累情况分为A1、A2及A3型;Stanford B型根据降主动脉扩张部位分为B1、B2及B3型;根据病因及弓部病变情况又分为C型(复杂型)和S型(简单型);临床诊断时根据实际情况组合确定,如A1C型、B2S型。具体分型方法详见《主动脉夹层诊断与治疗规范中国专家共识》 [ 17 ] 。(4)其他:2019年,欧洲心胸外科学会(European Association for Cardio-Thoracic Surgery,EACTS)与欧洲血管外科学会(European Society for Vascular Surgery,ESVS)胸主动脉疾病管理专家共识新增non-A-non-B型AD,用于描述内膜撕裂始于主动脉弓的AD [ 18 ] ;2020年,美国血管外科学会(Society for Vascular Surgery,SVS)与美国胸外科医师协会(Society of Thoracic Surgeons,STS)提出了根据内膜撕裂位置及AD近远端延伸范围的分型方法 [ 19 ] ;2024年,EACTS/STS指南 [ 20 ] 更新了基于AD类型、灌注不良的新分类方法。目前,DeBakey分型及Stanford分型仍是AD分型的基石,但随着对疾病认识的加深,国际权威机构对于AD疾病评估和手术策略制定的关联紧密性愈发关注。
AD的分期通常根据发病时间进行,但目前国内外尚无统一界定。传统分期方法将AD分为急性期和慢性期,发病时间≤14 d为急性期,发病时间>14 d为慢性期。国内专家推荐的AD分期方法为:发病时间≤14 d为急性期,发病时间15~90 d为亚急性期,发病时间>90 d为慢性期 [ 17 ] 。
四、流行病学及病因
目前,妊娠合并胸主动脉疾病相关的流行病学研究较少。妊娠合并胸主动脉扩张或胸主动脉瘤常无明显症状,患者多以AD等危重心血管事件就诊。欧美国家报道,妊娠期AD的发病率为(1.45~3.90)/10 000,为正常非妊娠人群的7~12倍 [ 21 ] 。AD患者中,妊娠期妇女占0.1%~0.4% [ 22 , 23 , 24 ] ;AD孕妇中,Stanford A型AD约占80%,Stanford B型AD约占20% [ 11 , 25 ] 。妊娠合并胸主动脉疾病患者合并遗传性结缔组织病约占60%,主动脉瓣二瓣化畸形(bicuspid aortic valve,BAV)约占5% [ 25 , 26 , 27 ] 。AD可能在整个妊娠期或产后数周内发生,70%发生于妊娠晚期或产后12周内(平均发病孕周31周),MFS孕妇的发病孕周更早 [ 26 , 27 , 28 , 29 , 30 ] 。虽然妊娠合并AD的救治有了长足进步,但孕产妇和胎儿的死亡率仍然较高,分别为16%和40% [ 12 ] 。
妊娠合并胸主动脉疾病主要有以下危险因素:(1)增加主动脉壁张力的各种因素:如妊娠期高血压疾病、主动脉缩窄、外伤等;(2)导致主动脉壁结构异常的疾病:MFS、Loeys-Dietz综合征(Loeys-Dietz syndrome,LDS)、血管型Ehlers-Danlos综合征(vascular Ehlers-Danlos syndrome,vEDS)等遗传性结缔组织疾病、BAV、家族性遗传性胸主动脉瘤(nonsyndromic heritable thoracic aortic disease,nsHTAD)和大动脉炎等 [ 24 , 27 , 31 , 32 ] 。
五、妊娠合并胸主动脉疾病的诊断与评估
(一)临床表现
1. 症状:胸主动脉瘤以主动脉根部和升主动脉瘤较为常见。除发展为急性主动脉综合征或发生主动脉破裂外,胸主动脉瘤早期多无明显临床表现,常于体检时偶然发现,也可随着动脉瘤增大压迫周围组织和器官,出现不同程度的疼痛和压迫所致的相关症状。主动脉根部瘤常合并主动脉瓣关闭不全,可出现心功能不全或心绞痛症状。
80%以上AD患者存在疼痛症状,常表现为撕裂样或针刺样持续性难以忍受的锐痛 [ 33 , 34 ] 。Stanford A型AD常表现为前胸痛或背痛,Stanford B型AD则表现为背痛或腹痛。AD累及主动脉近端和心脏时可出现急性主动脉瓣关闭不全、心肌梗死、心律失常等表现,重者可出现心力衰竭和(或)心源性休克;累及主动脉其他重要器官分支血管则可出现相应器官缺血或灌注不良表现,如晕厥、截瘫、无尿、黑便或血便、下肢麻木或疼痛等 [ 17 ] 。部分患者临床表现不典型或不明显,容易误诊或漏诊,常被误诊为妊娠反应、子痫、羊水栓塞或肺栓塞等。
2. 体征:对于妊娠合并胸主动脉疾病患者,除胸主动脉疾病所致的体征如上下肢或双侧血压不对称、心肺听诊异常以及其他器官或肢体受累体征外 [ 17 ] ,应注意其是否存在遗传性结缔组织病相关体征。MFS常伴有胸廓畸形、四肢过长、蜘蛛指(趾)、晶状体脱位、脊柱侧弯等特点 [ 35 ] ;vEDS以皮肤及血管脆弱、皮肤弹性过度及关节活动度过大为特征 [ 36 , 37 , 38 ] ;Turner综合征的特点为身材矮小、生殖器及第二性征不发育 [ 39 , 40 ] ;LDS具有动脉迂曲、漏斗胸或鸡胸、眼距过宽、悬雍垂裂等MFS样体征 [ 31 , 41 ] 。部分遗传性结缔组织病患者存在明确家族史。另外,考虑到胎盘血液供应主要来自起源于髂内动脉的分支子宫动脉,还应评估髂动脉受累对胎盘血流的影响。
(二)辅助检查
1. 实验室检查:血常规和血型、生化全套、凝血五项、心肌酶和心肌标志物、肌红蛋白、血气分析等常规的实验室检查有助于妊娠期胸主动脉疾病的鉴别诊断及器官功能评估。妊娠合并AD的术前实验室检查推荐详见相关诊疗规范 [ 17 ] 。但值得注意的是,由于D-二聚体在妊娠期内会有生理性升高,因此不推荐D-二聚体作为诊断及鉴别诊断妊娠期胸主动脉疾病的有效实验室指标 [ 42 ] 。
2. 影像学检查:临床上常用于胸主动脉疾病诊断的影像学检查技术有超声心动图、计算机断层扫描血管成像(computed tomography angiography,CTA)、磁共振成像(magnetic resonance imaging,MRI)、X线胸片和血管造影。影像学检查需评估的具体内容详见相关诊疗规范 [ 7 ] 。
(1)超声心动图:便携性强、无创伤、无辐射,可快速评价心功能、冠状动脉、主动脉瓣功能及主动脉窦受累情况,可用于各种状态患者的围术期评估。推荐作为妊娠合并胸主动脉疾病患者的首选检查方法 [ 43 ] 。但该检查对主动脉弓及胸降主动脉病变的诊断准确性较差,可考虑经食道超声心动图检查以提高诊断准确性。对于存在急性胸痛的患者应慎重选择经食道超声心动图 [ 1 ] 。
(2)CTA:对主动脉疾病诊断的准确性优于超声心动图,常作为AD的首选检查方法 [ 1 , 17 ] 。但考虑到胎儿辐射暴露可能导致不可预估的不良影响,除非高度怀疑急性主动脉综合征等危及孕妇生命的紧急情况,否则一般不作为孕产妇的常规检查 [ 32 , 44 ] 。
(3)MRI:对于妊娠、碘过敏、肾功能损害及甲状腺功能亢进者,MRI可作为首选检查方法 [ 17 , 32 , 43 ] 。MRI对胸主动脉疾病的诊断效率与CTA相似。但MRI扫描时间较长,部分患者难以配合、耐受,且应注意相关检查禁忌证。
(4)其他:X线胸片和血管造影在妊娠妇女中应慎用。
妊娠合并胸主动脉疾病的诊断与评估专家建议见 表2 。
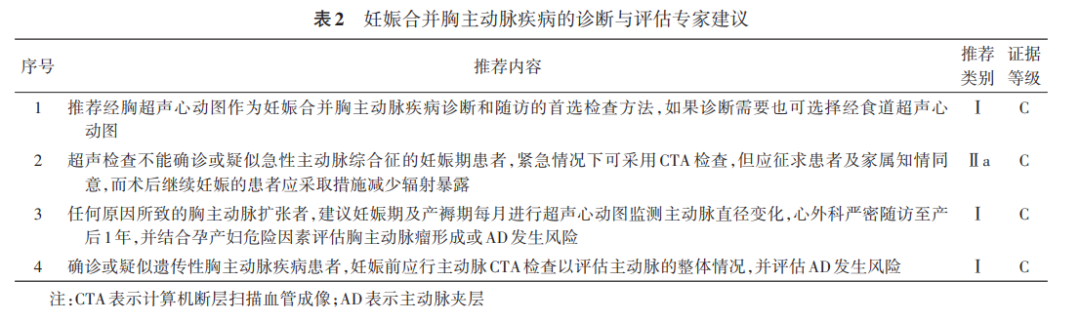
六、妊娠合并胸主动脉疾病的治疗与处理
(一)胸主动脉扩张或胸主动脉瘤
1. 合并遗传性结缔组织病:遗传性结缔组织病是导致妊娠期胸主动脉疾病的主要病因,其中,MFS是主要的遗传异常,占50%~68% [ 26 , 27 , 29 , 45 ] 。主动脉根部扩张或主动脉根部瘤是MFS早期的心血管系统表现,如未行有效干预可发生AD等严重并发症 [ 27 , 46 ] 。WHO根据主动脉根部直径制定了MFS妇女妊娠风险分级和治疗推荐 [ 47 ] 。但对于育龄期MFS患者,即使主动脉根部直径正常,妊娠期仍存在1%发生AD或其他心脏并发症的可能;当主动脉根部直径≥4.0 cm时,AD发生风险增加4%~10% [ 30 ] 。因此,美国和欧洲权威学术机构最新指南 [ 1 , 4 , 20 ] 一致推荐,对于计划妊娠且主动脉根部直径为4.0~4.4 cm的MFS妇女,可考虑在妊娠前进行预防性主动脉手术,尤其是存在主动脉扩张速度≥0.3 cm/年或有AD家族史等高危因素者;而对于主动脉根部直径≥4.5 cm的MFS妇女,则建议先行预防性主动脉手术。
其他遗传综合征如LDS、vEDS、Turner综合征等常伴有胸主动脉扩张或胸主动脉瘤,且AD发生风险高 [ 31 , 48 , 49 , 50 ] 。此类患者升主动脉直径≥4.5 cm或主动脉直径指数(主动脉根部或升主动脉直径与体表面积之比)≥2.5 cm/m 2时可根据患者病情考虑行预防性手术 [ 2 ] 。对于已经行主动脉根部手术的患者,远期至少发生一次主动脉事件(AD、再次手术或破裂)的比例为21.4% [ 51 ] 。
2. 合并BAV:约50%的BAV或主动脉瓣狭窄患者可合并升主动脉扩张或胸主动脉瘤,不同瓣膜融合亚型造成主动脉扩张的部位有所不同 [ 52 , 53 ] 。BAV合并升主动脉瘤发生AD的风险低于遗传性结缔组织病所致的主动脉扩张,但当升主动脉直径≥5.0 cm时(mWHO风险Ⅳ级)将极大增加孕产妇的死亡风险 [ 47 ] 。因此,此类患者仍应考虑预防性手术治疗 [ 1 ] 。
3. 单纯胸主动脉扩张或胸主动脉瘤:除外遗传性结缔组织病、nsHTAD [ 54 ] 等遗传性疾病,对于单纯胸主动脉扩张或胸主动脉瘤妊娠期患者,当升主动脉直径≥5.0 cm时应考虑预防性手术治疗。另外,当此类患者主动脉扩张速率过快时(≥0.5 cm/年),也应考虑预防性手术治疗 [ 1 ] 。
必须指出的是:对于计划妊娠的育龄期妇女,明确近端主动脉病变预防性手术干预的时机是十分复杂的,应由心脏病学、妇产科、医学遗传学和经验丰富的心外科医师所组成的妊娠合并胸主动脉疾病多学科团队共同决策;同时,还应综合考虑特定遗传性疾病类型、基因变异类型、主动脉扩张速度、家族史和表型等多种因素的影响 [ 1 , 4 , 47 ] 。胸主动脉扩张或胸主动脉瘤预防性干预时机的专家建议见 表3 。

4. 妊娠合并胸主动脉扩张或胸主动脉瘤的分娩方式:妊娠期主动脉直径增加与AD发生风险相关性较强,但缺乏不同分娩方式发生主动脉不良事件的研究 [ 1 , 30 ] 。结合国际指南及国内临床实践,建议主动脉根部直径<4.0 cm的孕妇,可在严密监护下阴道分娩;主动脉根部直径≥4.5 cm或存在AD病史的孕妇,建议剖宫产术分娩;主动脉根部直径4.0~4.4 cm的孕妇,应由妊娠合并胸主动脉疾病多学科团队充分评估风险后选择行剖宫产术分娩,或严密监护下行分娩镇痛的阴道分娩(阴道助产缩短第二产程) [ 1 ] 。但无论采用何种分娩方式,均应提前告知孕妇及其家属分娩过程中可能发生AD或主动脉破裂等风险,尽可能在心外科医师在场的情况下分娩 [ 3 , 55 ] 。妊娠合并胸主动脉扩张或胸主动脉瘤分娩方式的专家建议见 表4。

(二)AD
1. 基础治疗原则:妊娠合并AD的基础治疗应遵循非妊娠期AD的诊疗原则,其目的是通过药物有效镇痛、控制心率和血压,降低主动脉剪应力和主动脉破裂的风险 [ 7 , 25 ] 。可适当肌内注射或静脉输注阿片类药物(吗啡、哌替啶)减轻疼痛,降低交感神经兴奋导致的心率和血压升高,提高控制心率和血压的效果。初步治疗目标为控制收缩压至100~120 mmHg(1 mmHg=0.133 kPa)、心率60~80次/min [ 25 ] 。在实施药物治疗时,应警惕药物毒性对胎儿的影响,如血管紧张素转换酶抑制剂、血管紧张素受体阻滞剂类降压药是孕妇禁忌 [ 56 ] 。妊娠期血压管理的用药方案及注意事项详见《妊娠期高血压疾病诊治指南(2020)》 [ 57 ] 和《妊娠期高血压疾病血压管理中国专家共识》 [ 58 ] 。
2. 妊娠合并AD的手术干预策略:一旦孕产妇确诊AD,应引起高度重视并立即启动绿色通道,尽快接受综合治疗。需急诊手术治疗的妊娠合并胸主动脉疾病(如急性Stanford A型AD等),应尽可能缩短手术准备时间 [ 27 , 59 ] 。妊娠合并AD的外科手术策略应由妊娠合并胸主动脉疾病多学科团队结合孕妇所处妊娠阶段、AD类型和胎儿宫内状态等因素综合评估,并在征求孕妇及其家属知情同意后制定诊疗方案。见 图1 。
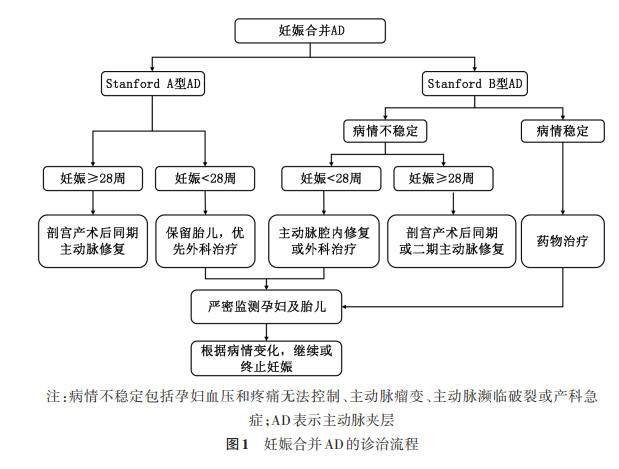
(1)Stanford A型AD:妊娠合并Stanford A型AD极为凶险,患者随时可能因AD破裂、失血性休克、器官缺血或灌注不良等并发症而死亡。急性Stanford A型AD的急诊手术指征同样适用于妊娠合并Stanford A型AD。应以挽救孕妇生命为主,在此前提下尽可能保证胎儿存活 [ 22 , 27 , 28 ] 。妊娠合并Stanford A型AD的外科手术策略制定应综合考虑妊娠合并胸主动脉疾病多学科团队会诊意见、胎龄、孕妇及家属的意愿后决定。
由于胎龄<28周胎儿的整体存活率低(尤其是<26周),妊娠早期、中期的治疗策略应优先挽救母亲生命,但应充分告知CPB后继续妊娠期间可能导致胎儿丢失、极早产儿和孕产妇死亡的风险 [ 60 , 61 ] 。若孕妇主动脉术后继续妊娠意愿强烈,则应征询妊娠合并胸主动脉疾病多学科团队意见,术中、术后进行胎儿监测,并根据胎儿状况决定是否终止妊娠。根据《早产临床防治指南(2024版)》 [ 62 ] ,26~28周龄的有生机儿存活率已超过80%。因此,妊娠合并胸主动脉疾病多学科团队必须全面权衡孕妇和胎儿的存活风险后制定治疗策略。具备早产儿救治条件的地区和机构,在孕妇及其家属充分知情同意后,可考虑先行剖宫产术娩出胎儿,然后同期行外科手术,并积极救治26~28周龄的有生机儿。对于妊娠晚期的孕妇,建议剖宫产术后同期行外科手术 [ 27 , 60 , 63 ] 。必须强调的是,剖宫产术应在全身肝素化和CPB开始前进行,以减小子宫致命性出血的可能。
为尽可能保证Stanford A型AD患者术后胎儿存活,可采取以下措施 [ 26 , 29 ] :①术中采用股动脉及腋动脉同时插管以保证胎盘灌注;②若夹层局限于升主动脉应尽量避免低温停循环手术;③为避免口服抗凝药物对胎儿的影响,如有可能尽量行保留主动脉瓣或生物瓣置换的主动脉根部手术;④术中尽可能缩短CPB时间;⑤首选顺行性脑灌注。另外,对于主动脉弓部受累的Stanford A型AD孕妇,主动脉弓部重建策略存在较大争议。单纯升主动脉或主动脉根部(±部分主动脉弓置换)手术较为简单、安全,可能有利于胎儿存活,但增加了孕妇主动脉并发症的远期风险;全主动脉弓替换+支架象鼻手术(孙氏手术)有利于远端降主动脉重塑,可降低再次手术率,但因停循环时间较长,胎儿存活率低 [ 26 , 29 , 60 , 64 ] 。建议根据术者经验及患者病情,在保证孕妇安全的前提下,选择合适的主动脉根部及主动脉弓部重建方法。
对于妊娠晚期Stanford A型AD孕妇,剖宫产术后同期行主动脉手术,无需考虑对胎儿的影响,其CPB策略、动脉插管方式、主动脉根部及主动脉弓部重建策略可参考非妊娠期Stanford A型AD外科治疗处理原则 [ 17 ] 。临床上65%以上的妊娠合并Stanford A型AD患者在剖宫产术后同期或分期行主动脉手术 [ 27 ] 。Stanford A型AD外科手术的常见并发症及其处理参考相关诊疗规范 [ 17 ] 。另外,考虑到同期剖宫产术后需肝素化下行外科手术,发生严重产后出血的可能性大,剖宫产术中可考虑放置宫腔球囊压迫止血联合小剂量缩宫素预防产后出血,术后24 h内取出球囊,如果发生宫缩乏力或者出血难以控制也可实施子宫捆绑术或子宫动脉结扎术,并继续严密观察出血情况。另外,禁忌使用甲基麦角新碱、卡前列素氨丁三醇。见 表5 。
(2)Stanford B型AD:Stanford B型AD的凶险程度较Stanford A型AD低。药物治疗是Stanford B型AD的基本治疗方式,也是此类稳定型患者的首选治疗方式 [ 1 , 26 ] 。2022年美国指南 [ 1 ] 和2024年欧洲指南 [ 20 ] 均建议,妊娠合并Stanford B型AD者需严格控制心率和血压。目前,国内外关于妊娠合并Stanford B型AD治疗的经验较少,具体治疗方案应根据孕妇的病情是否稳定和所处妊娠阶段制定 [ 26 , 29 ] 。①妊娠<28周:如果孕妇血压和疼痛无法控制、发生主动脉瘤变、主动脉濒临破裂或产科急症,应接受药物治疗的同时考虑急诊行主动脉腔内修复术或外科手术;②妊娠≥28周:可视孕妇及胎儿情况进行保胎或剖宫产术,然后同期或二期行介入或外科手术 [ 65 ] 。国内报道腔内修复治疗妊娠晚期和产褥期Stanford B型AD早期和中期效果满意,其远期效果及安全性有待更多的研究验证 [ 66 , 67 ] 。对于胎儿未娩出的孕妇,应尽量减少诊疗过程中的辐射暴露。见 表6。

(三)CPB与妊娠期胸主动脉外科手术
CPB对孕妇的影响与非妊娠期患者相似,但对胎儿大脑等重要器官的发育产生负面影响,并可能导致流产、胎儿窘迫、胎死宫内等不良预后。CPB期间子宫-胎盘灌注不足,胎盘血流量和氧交换减少,导致胎儿缺氧、心输出量下降。胎盘的血液供应取决于母体循环和胎儿循环,CPB流量和平均动脉压是影响胎儿氧合最重要的因素 [ 60 , 61 , 68 ] 。CPB导致盘灌注不足的因素包括:低灌注压、血液稀释、血管活性物质释放、血管扩张药物、非搏动性血流、子宫收缩和低温等 [ 68 , 69 ] 。因此,为降低胎儿宫内缺氧风险,建议应尽量缩短CPB时间,维持高流量(>2.5 L·min -1·m -2)、高灌注压(>70 mmHg)、血细胞压积>0.25和采用搏动性血流 [ 27 , 29 , 60 ] 。
另外,低温对胎儿的影响较大。浅低温(28.1~34.0 ℃)条件下,胎儿能自主调节心率并耐受CPB手术。因此,对于妊娠早期及中期的胎儿,常温或浅低温主动脉根部或升主动脉手术是相对安全的,但进一步降低CPB温度可能会对胎盘功能和胎儿造成不良影响 [ 27 , 60 , 68 ] 。而主动脉弓部手术涉及低温停循环操作,术后胎儿存活率较低 [ 27 , 29 , 70 ] 。目前,对于涉及主动脉弓的非妊娠期Stanford A型AD患者,国内专家共识推荐中低温停循环下行孙氏手术 [ 17 ] 。但妊娠期需同时考虑孕妇及胎儿预后,是否应该实施低温停循环手术尚存在争议。建议根据孕妇的意愿、病情、胎儿状态及医疗机构的技术水平综合考虑。对于有强烈保胎意愿、胎儿状况良好且病变较为局限的孕妇,建议术中尽可能避免低温停循环。见 表7 。

(四)妊娠期胸主动脉外科手术的围术期麻醉管理策略
妊娠期胸主动脉外科手术对麻醉医师的挑战是巨大的。围术期麻醉管理需要同时考虑麻醉药物或其配伍对母亲和胎儿的双重影响,且涉及整个妊娠期和哺乳期,在妊娠早期尤为突出 [ 45 , 71 ] 。虽然美国出生缺陷预防研究证实,各种麻醉技术中常规使用的麻醉药物剂量是安全的,但部分麻醉药物仍可能作用于妊娠早期的快速分裂细胞,导致胎儿器官发育障碍 [ 72 ] 。而妊娠中期、晚期孕妇需剖宫产术后同期行主动脉手术,如何合理应用麻醉药物安全完成剖宫产术与主动脉手术的衔接,以及管理困难气道是此类患者围术期麻醉管理的重点及难点 [ 73 , 74 ] 。另外,围术期疼痛将引发强烈应激反应并导致病理性宫缩,增加胎儿早产、宫内窘迫等风险。因此,围术期麻醉管理应采用多模式策略,推荐高选择性、小剂量起效且对血流动力学影响小的镇痛药物,将药物对母亲和胎儿的副作用最小化 [ 45 , 75 ] 。总之,临床实践中需结合多学科团队协作,麻醉药物和血管活性药物种类及剂量,精细调控麻醉深度,密切监测母儿安全。见 表8 。

七、妊娠指导
(一)妊娠合并胸主动脉疾病的遗传咨询
妊娠合并胸主动脉疾病与MFS、nsHTAD、LDS和vEDS等密切相关 [ 31 ] 。目前有11个基因已被证实与胸主动脉疾病的发生存在较强关联,包括FBN1、LOX、COL3A1、TGFBR1、TGFBR2、SMAD3、TGFB2、ACTA2、MYH11、MYLK和PRKG1基因 [ 76 ] 。6%~8%的遗传性胸主动脉疾病家系中存在FBN1、TGFBR1、TGFBR2、SMAD3和TGFB2等基因突变,但其家系成员并未表现出MFS或LDS特征 [ 77 , 78 , 79 , 80 ] 。而ACTA2、MYH11、MYLK、LOX和PRKG1基因突变可导致遗传性胸主动脉疾病,但不伴有MFS或LDS的显著特征 [ 81 , 82 ] 。另外,BAV和动脉缩窄的基因遗传倾向不是十分明确,但如果夫妇双方均存在已知基因突变,则建议行产前诊断检测胎儿的突变。羊水穿刺和绒毛膜绒毛穿刺可以用于有遗传倾向的胸主动脉疾病孕妇的胎儿检测 [ 83 ] 。综上,对mWHO风险≥Ⅱ~Ⅲ级的妊娠前和妊娠期女性,尤其是可疑遗传性结缔组织病或有nsHTAD家族史者,完善临床判定(依据2010年修订版Ghent标准 [ 84 ] ),建议进行遗传学咨询,全面了解其家族史,确定家族先证者,并进行必要的遗传学检查或基因诊断以制订合理的治疗策略和评估疾病遗传风险 [ 35 , 76 , 85 ] 。诊断及筛查的相关指导可参见《遗传性胸主动脉瘤/夹层基因检测及临床诊疗专家共识》 [ 86 ] 。见 表9 。

(二)再次妊娠的指导
虽然预防性手术可防止近端AD,但是MFS和nsHTAD患者行主动脉根部替换术后仍存在发生远端主动脉病变的风险 [ 1 , 87 ] ;而明确有TGFBR1和TGFBR2基因致病变异的LDS妇女,AD发生风险则可能更高 [ 88 ] 。因此,对于患有遗传性结缔组织病的育龄期女性,再次妊娠前应充分征求心外科、妇产科、遗传学等专家意见,做好妊娠前咨询和风险评估,若存在明确致病基因突变,可选择辅助生殖联合单基因遗传病胚胎植入前遗传学检测技术受孕。对于无再次妊娠意愿的患者,应做好避孕措施,建议避免使用含雌激素和孕激素的口服避孕药,推荐使用避孕套等物理屏障方法。对于计划长期避孕的患者,可以考虑长效可逆避孕方法 [ 89 ] 。
特定胸主动脉疾病孕产妇的死亡率或妊娠期严重并发症的发生风险极高,建议避免妊娠。主动脉直径≥4.5 cm的MFS、主动脉直径≥5.0 cm的BAV、主动脉尺寸指数≥2.5 cm/m 2的Turner综合征、vEDS、未经手术修复的严重主动脉缩窄、主动脉直径≥5.0 cm的胸主动脉扩张或胸主动脉瘤、有AD病史或残余AD所致的主动脉直径持续扩张者,一旦发现妊娠应建议终止妊娠 [ 4 ] 。
八、监测与随访
无论是否行手术治疗、是否终止妊娠,妊娠合并胸主动脉疾病患者均需密切随访。对于未行手术治疗的妊娠期胸主动脉疾病患者,建议妊娠期和产褥期内每月进行1次超声心动图检查,需监测主动脉病变进展情况至产后1年 [ 3 ] 。如果主动脉直径较大或妊娠合并胸主动脉疾病多学科团队认为AD潜在发生风险升高,应增加检查频率,必要时可行手术干预 [ 47 ] 。对于行主动脉手术的妊娠期患者,还需每月行胎儿超声检查直至分娩,以监测胎儿发育状况,若发现胎儿异常或其他严重并发症,应终止妊娠;而对于已行主动脉手术且终止妊娠的患者,其随访原则同非妊娠患者的主动脉术后随访。如无特殊紧急情况,随访期间应尽量避免胎儿的辐射暴露。
随访期间应积极控制主动脉疾病的危险因素,包括规律服用降心率、降压药物严格控制患者的血压、心率,其目标值建议分别控制在120/80 mmHg以下和60~80次/min。β受体阻滞剂可能降低主动脉扩张速度,并改善患者远期生存率 [ 90 ] 。特别是对于MFS患者,建议服用β受体阻滞剂降低主动脉根部扩张速度。但是,妊娠期服用β受体阻滞剂时应监测胎儿的生长情况 [ 32 , 91 , 92 ] 。
妊娠合并胸主动脉疾病患者需要根据个体情况来决定产后能否母乳喂养。在做出决策之前,妊娠合并胸主动脉疾病多学科团队应考虑所有相关的健康和安全因素,并与产妇及家属充分沟通。存在心功能不全或心力衰竭的产妇不建议母乳喂养 [ 92 ] 。妊娠合并胸主动脉疾病的产后指导可参见《妊娠合并心脏病的诊治专家共识(2016)》 [ 58 ] 。
执笔人: 陈苏伟(首都医科大学附属北京安贞医院主动脉外科中心)、张豪锋(首都医科大学附属北京安贞医院妇产科)、钟永亮(首都医科大学附属北京安贞医院主动脉外科中心)、乔志钰(首都医科大学附属北京安贞医院主动脉外科中心) 共识专家组成员(按姓氏拼音排序): 卞晓明(大连医科大学第一附属医院心脏外科)、陈海生(广州市第一人民医院心脏大血管外科)、陈良万(福建医科大学附属协和医院心脏外科)、蔡雁(哈尔滨医科大学附属第四医院产科)、丁新(首都医科大学附属北京妇产医产科)、段维勋(空军军医大学第一附属医院心血管外科)、董念国(华中科技大学同济医学院附属协和医院心脏大血管外科)、范瑞新(广东省人民医院心脏外科)、葛静(沈阳菁华医院生殖中心)、高婉丽(首都医科大学附属北京天坛医院妇产科)、谷天祥(中国医科大学附属第一医院心脏外科)、韩凤珍(广东省人民医院产科)、韩林(海军军医大学第一附属医院心血管外科)、黑飞龙(首都医科大学附属北京安贞医院体外循环科)、黄福华(南京市第一医院心脏大血管外科)、黄连军(上海德达医院影像与介入中心)、黄凌瑾(中南大学湘雅医院心血管外科)、柳克祥(吉林大学第二医院心血管外科)、赖颢(复旦大学附属中山医院心脏外科)、林建华(上海交通大学医学院附属仁济医院妇产科)、龙燕(首都医科大学附属北京友谊医院妇产科)、李燕娜(首都医科大学附属北京安贞医院妇产科)、刘永民(首都医科大学附属北京安贞医院主动脉外科中心)、刘志刚(泰达国际心血管病医院心脏外科)、金沐(首都医科大学附属北京安贞医院麻醉中心)、金振晓(空军军医大学第一附属医院心血管外科)、苗齐(泰达国际心血管病医院心脏外科)、潘晓玉(中日友好医院妇产科)、苏丕雄(首都医科大学附属北京朝阳医院心脏外科)、孙立忠(上海德达医院心脏大血管外科)、孙图成(广东省人民医院心脏外科)、孙晓刚(中国医学科学院阜外医院血管外科中心)、孙志华(北京市朝阳区妇幼保健院妇产科)、唐皓(中南大学湘雅二医院心血管外科)、徐东(首都医科大学宣武医院心脏外科)、吴龙(华中科技大学同济医学院附属协和医院心脏大血管外科)、王嵘(首都医科大学附属北京安贞医院麻醉中心)、王晟(首都医科大学附属北京安贞医院麻醉中心)、王军(大连医科大学第二附属医院妇产科)、王宪珍(辽宁省朝阳市中心医院妇产科)、魏翔(华中科技大学同济医学院附属同济医院心脏大血管外科)、武忠(四川大学华西医院心脏大血管外科)、武婷(天津市胸科医院心血管外科)、谢宝栋(哈尔滨医科大学附属第一医院心脏大血管外科)、杨冬(首都医科大学附属北京安贞医院妇产科)、赵鑫(山东大学齐鲁医院心血管外科)、张大伟(首都医科大学附属北京安贞医院妇产科)、张军(首都医科大学附属北京安贞医院妇产科)、张卫社(中南大学湘雅医院产科)、张喆(北京大学第三医院心脏外科)、郑宝石(广西医科大学第一附属医院心血管外科)、郑军(中国医学科学院北京协和医院心脏外科)、郑铁(首都医科大学附属北京安贞医院主动脉外科中心)、周成斌(广东省人民医院体外循环科)、朱俊明(首都医科大学附属北京安贞医院主动脉外科中心) 参考文献 略 利益冲突 所有作者声明无利益冲突
