中华医学会
地址: 中国北京东四西大街42号
邮编: 100710
多发性线粒体功能障碍综合征1型1例
【摘要】报道1例新生儿期起病的多发性线粒体功能障碍综合征1型,以反应弱、纳差、血乳酸增高为主要表现,头颅MRI提示脑白质,基因测序提示NFU1基因外显子c.167-1G>T纯合变异。总结患儿临床特点、诊断和治疗过程,以加强临床医生对本病的认识。
病例资料
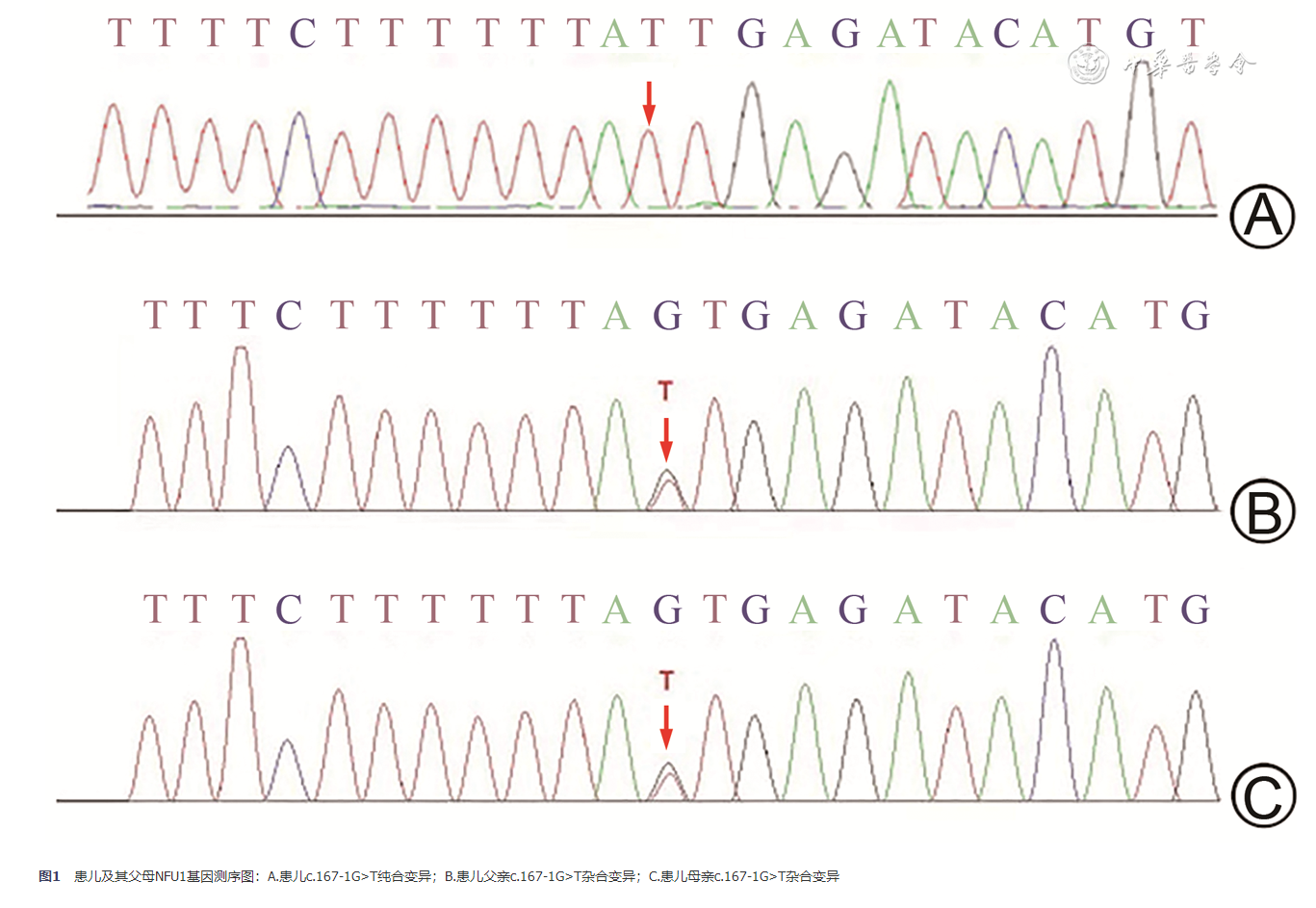
患儿女,藏族,30 d(校正胎龄40周),因“神倦、少吃少动15 d”入院。患儿系第1胎第1产,胎龄35+5周因“母重度子痫前期”剖宫产娩出,出生体重1 750 g,无围产期缺氧史,生后曾因“低出生体重儿、低血糖症”入院,生后20 min末梢血糖2.1 mmol/L,入院后患儿低血糖很快纠正,日龄12 d出院(体重1 810 g),院外纯母乳喂养。近15 d来患儿出现神倦、少吃少动,伴体重增长缓慢,无发热、呕吐、腹胀及惊厥表现。否认家族遗传病史。入院查体:体重1 830 g,反应差,哭声细小,皮肤干燥伴脱屑,中度黄染。呼吸不规则,可见轻度吸气性三凹征,双肺听诊无异常,心腹无异常。四肢无肌张力减低,原始反射减弱。辅助检查:血常规、C反应蛋白、降钙素原、肝肾功能、甲状腺功能、胰岛素水平、血TORCH检测均无异常,血清葡萄糖0.94 mmol/L,钾6.0 mmol/L,总胆红素256 μmol/L,间接胆红素升高为主,血乳酸11.9 mmol/L;头颅、心脏、腹部超声大致正常;振幅整合脑电图:未监测到惊厥发作,背景活动不连续,上边界<10 μv,下边界<5 μv,未见明显睡眠觉醒周期;头颅MRI:双侧大脑脑白质T1WI普遍信号减低,T2WI信号增强,灰白质界限不清,DWI信号增高,累及双侧尾状核头部及双侧基底节区、胼胝体,双侧丘脑信号未见异常;尿有机酸分析:乳酸、丙酮酸升高明显,提示酮尿;血串联质谱分析:丙氨酸增高。全外显子组基因测序:患儿NFU1基因外显子c.167-1G>T 纯合变异,患儿父母NFU1基因上均存在c.167-1G>T杂合变异(图1)。诊断:多发性线粒体功能障碍综合征(multiple mitochondrial dysfunction syndrome,MMDS)1型。入院后给予补液、纠正低血糖和代谢性酸中毒,口服辅酶Q10、左卡尼汀,静脉点滴精氨酸等治疗,患儿低血糖、电解质紊乱好转,尿量逐渐从1.7 ml/(kg·h)增加至3.5 ml/(kg·h),但仍纳差、反应弱,血乳酸增高,波动于10.2~12.5 mmol/L。住院第10天家长要求自动出院。出院后患儿纳奶量逐渐减少,呼吸逐渐减弱,于日龄50 d死亡。
讨论 MMDS是由于线粒体基因或编码线粒体的基因发生致病变异而导致的线粒体功能障碍,进而出现能量代谢紊乱的一种先天性代谢缺陷疾病,为常染色体隐性遗传病。2011年首次出现基因变异致病的报道[1],临床上根据基因分为6型,其中MMDS1型是由2p13.3号染色体上的NFU1基因变异导致。MMDS多在婴儿早期起病,临床表现有喂养困难、呼吸衰竭、嗜睡、发育迟缓或倒退、肌张力低、婴儿脑病和肺动脉高压等。辅助检查方面主要有血清乳酸、甘氨酸及丙酮酸水平升高。脑MRI受累的表现形式与基因变异类型有关,常见脑白质病变,也可见基底节神经节病变、小脑和视神经萎缩[2]。本例患儿以神倦、喂养困难起病,血乳酸明显升高,尿乳酸、丙酮酸升高,头颅MRI提示脑白质病变,全外显子检测发现NFU1基因c.167-1G>T纯合变异,故诊断MMDS1型明确。 本病无有效治疗药物[3],以对症治疗为主,包括补充呼吸链辅因子如辅酶Q10和维生素B2,抗氧化剂如维生素E,同时可补充精氨酸和左卡尼汀,供给充足营养,维持内环境稳定,同时避免误吸。患儿常于婴儿早期死亡,生存时间大部分仅有0~9个月,存活15个月以上的报道目前仅有3例[4]。本例患儿明确诊断后虽积极对症治疗,但纳差、高乳酸血症难以纠正,家长放弃治疗后患儿很快死亡。对于血尿乳酸、丙酮酸升高伴头颅MRI脑白质病变的患儿,需考虑先天性代谢异常、线粒体脑病可能,应积极完善血串联质谱、尿有机酸分析和基因测序等检查尽快明确诊断,早干预、早治疗,争取延长患儿生命。 引用本文: 杜维纳, 肖甜甜, 巨容, 等. 多发性线粒体功能障碍综合征1型1例 [J] . 中华新生儿科杂志, 2023, 38(1) : 49-50. DOI: 10.3760/cma.j.issn.2096-2932.2023.01.013.