中华医学会
地址: 中国北京东四西大街42号
邮编: 100710
孕产妇合并新型冠状病毒感染诊治推荐意见
摘要
为进一步科学、规范地做好孕产妇合并新型冠状病毒(简称新冠病毒)感染的诊治工作,在国家卫生健康委员会妇幼保健司指导下,中华医学会围产医学分会组织权威专家,依据国家卫生健康委员会《新型冠状病毒感染诊疗方案(试行第十版)》,结合孕产妇和新生儿特殊群体特点以及国内外诊治经验,研究制定了本指南,目的是有效地指导孕产妇新冠病毒感染的临床管理。
一、流行病学及预后
人群对新冠病毒普遍易感[1],孕产妇感染新冠病毒的发病率较普通人群未见明显增加[2]。妊娠可能会加重新冠病毒感染的临床病程,也可能出现重症[3-4]。
在全球新冠大流行期间,自然流产或出生缺陷的发生率并未升高[5]。新冠病毒感染孕妇发热及低氧血症可增加早产、胎膜早破和胎心率异常的风险[6];对于重症患者,分娩可以改善母体重度呼吸系统疾病的症状,部分孕晚期重型或危重型病例需要剖宫产终止妊娠[4,7-9]。新冠病毒感染孕妇合并子痫、溶血肝功能异常血小板减少综合征以及慢性高血压、子痫前期、多胎妊娠、脓毒症、休克、急性呼吸窘迫综合征、需要机械通气等增加胎儿不良结局的风险,发生死胎及新生儿窒息的风险较高[10-12]。
新冠病毒感染孕妇分娩的新生儿中,95%以上未感染且出生状态良好,新生儿感染多为生后接触感染者通过呼吸道或接触传播。
二、诊断标准
(一)临床表现及检查
1.临床表现:孕产妇新冠病毒感染的症状与普通人群相似,包括发热、乏力、鼻塞、咳嗽、肌痛、咽痛、流鼻涕,部分孕产妇有嗅觉、味觉减退或丧失以及结膜炎和腹泻等。最常见的临床症状为咳嗽和发热[13-14]。
2.实验室检查:(1)病原学检测:常用新冠病毒核酸/抗原(以下简称核酸/抗原)检测,其他还有病毒分离、特异性lgM和IgG抗体检测。(2)结合病情可以进行以下检查:血常规、凝血功能、心肌酶、肝功能、肾功能、细胞因子等。感染早期外周血白细胞计数正常或减少,可见淋巴细胞计数减少,部分患者可出现肝酶、乳酸脱氢酶、肌酶、肌红蛋白、肌钙蛋白和铁蛋白增高。多数患者C-反应蛋白和血沉升高。
3.影像学检查:胸部低剂量X射线和CT检查是评价新冠病毒感染者肺损伤的重要依据。妊娠中晚期在完善的放射防护条件下, 可进行胸部低剂量X射线或CT检查。
(二)临床诊断与分型
1.诊断:根据流行病史,出现临床表现,结合实验室、影像学检查资料,可以诊断妊娠合并新冠病毒感染。(1)具有新冠病毒感染的相关临床表现。(2)具有以下一种或以上病原学和血清学检查结果:①新冠病毒核酸检测阳性;②新冠病毒抗原检测阳性;③新冠病毒分离、培养阳性,恢复期新冠病毒特异性IgG抗体水平为急性期4倍或以上升高[13-15]。
2.分型:(1)轻型:临床症状轻微,影像学检查未见肺部感染表现。(2)中型:具有发热、呼吸道感染等症状,如持续高热>3 d,和/或伴有咳嗽和气促等,但呼吸频率<30次/min,静息状态下吸入空气时末梢血氧饱和度>93%;影像学检查可见特征性新冠病毒感染肺炎表现。(3)重型:符合下列任何一条且不能由其他原因解释:①呼吸窘迫,呼吸频率≥30次/min;②静息状态下动脉血氧饱和度≤93%;③动脉血氧分压/吸入氧浓度≤300 mmHg(1 mmHg=0.133 kPa);④临床症状进行性加重,肺部影像学检查显示24~48 h内病灶明显进展50%者。(4)危重型:有以下情况之一者,且不能由其他原因解释:①呼吸衰竭,需要机械通气;②出现休克;③合并其他器官功能衰竭需重症监护。
三、重症识别与处理
孕产妇合并新冠病毒感染时,可能增加住院以及入住重症监护病房的风险,极少数甚至导致死亡。若孕产妇存在未完成新冠病毒疫苗全程接种、高龄、肥胖、多胎妊娠,合并基础疾病如高血压、心脏病、慢性阻塞性肺病、糖尿病,以及妊娠合并症等因素,容易发生重型新冠病毒感染。
若孕晚期有以下情况应警惕病情恶化以及发生重症的可能:低氧血症或呼吸窘迫进行性加重、组织氧合指标(氧饱和度、氧合指数)恶化或乳酸进行性升高、外周血淋巴细胞计数进行性降低或炎症因子如白细胞介素-6、C-反应蛋白和铁蛋白等进行性升高,以及D-二聚体等凝血功能相关指标明显升高[16]。
四、孕期保健
(一)自我监测
新冠病毒感染孕妇应在加强自我防护的同时,注意自我健康监测[17]。监测的主要内容包括体温、心率、血压以及有无呼吸道感染症状。有条件者,还可监测末梢血氧饱和度[18]。孕晚期需关注胎动。
孕妇新冠病毒感染症状经对症处理不缓解,出现高热不退(热峰≥39 °C超过3 d)、呼吸困难、头晕或头痛加重、憋气、心悸、意识模糊等严重不适[19-21],或者出现胎动异常或消失,或出现阴道出血及流液、腹痛、血压升高等表现时,要及时就诊[22-23]。
(二)孕期检查的原则和时间点
根据孕妇具体情况,必要时可适当调整产前检查时间。但胎儿颈项透明层厚度超声检查、唐氏综合征血清学筛查、系统彩超等部分检查项目存在关键时间段,应与产前检查医院和医生沟通确定产前检查时间。
下列情况需前往门诊就医:(1)新冠病毒感染症状严重或经对症处理不缓解;(2)需要做不能再调整时间的产前检查项目;(3)出现产科指征如胎动异常或消失、阴道出血及流液、腹痛、血压升高等表现时。
就医时应注意规范佩戴N95口罩,尽量通过网上预约挂号、预约检查等,有条件者可通过线上医疗的形式咨询。
(三)药物治疗
1.对症治疗:孕产妇合并新冠病毒感染的对症治疗应权衡利弊,谨慎考虑其对孕产妇、胚胎/胎儿/新生儿/哺乳婴儿的影响,常用的对症治疗药物见表1[24-26]。
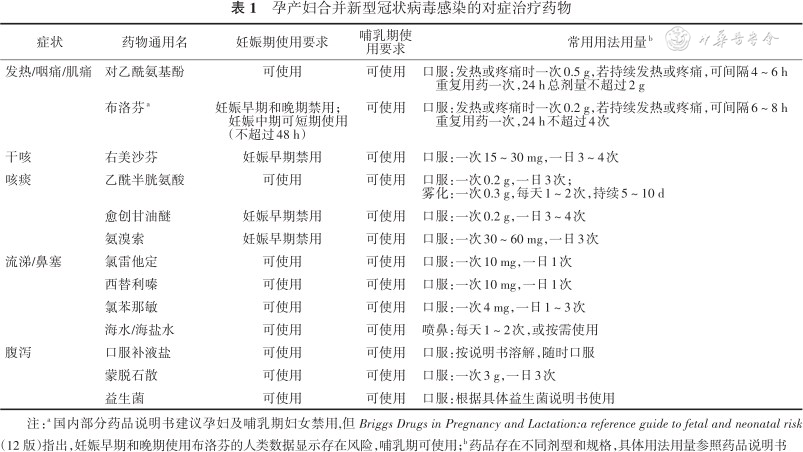
若使用复方感冒药,应注意对乙酰氨基酚每日总量不能超过2 g。由于部分复方感冒药含有不推荐妊娠及哺乳期使用的成分(如金刚烷胺、伪麻黄碱等),建议妊娠及哺乳期选择单一成分的药物对症治疗。
若选用中药治疗,须遵循中医辨证论治原则,个体化用药。应尽量规避妊娠禁忌药物,若确因病情需要,告知患者并知情同意后使用,但应严格掌握用药剂量及时间,以免伤胎、动胎。
一般不需使用抗菌药物。若合并细菌感染,需在医生指导下选择适宜抗菌药物,避免盲目或不恰当使用,尤其是联合使用广谱抗菌药物。
2.抗病毒治疗:抗病毒药物可降低伴有高危因素的轻至中型新冠病毒感染患者发展为重症的风险。国家卫生健康委员会《新型冠状病毒感染诊疗方案(试行第十版)》推荐口服抗病毒药物包括奈玛特韦/利托那韦组合包装、阿兹夫定片和莫诺拉韦胶囊[27]。
奈玛特韦片/利托那韦片组合包装适用人群为发病5 d以内的轻、中型且伴有进展为重症高风险因素的成年患者。用法:奈玛特韦 300 mg与利托那韦100 mg同时服用,每12小时1次,连续服用5 d。只有孕妇的潜在获益大于对胎儿的潜在风险时,才能在妊娠期间使用。若哺乳期使用,治疗期间以及治疗结束后7 d应暂停哺乳。中度肾功能损伤者应将奈玛特韦减半服用,重度肝、肾功能损伤者不应使用。使用前应详细阅读说明书,注意合并用药间的相互作用。
不建议在妊娠期和哺乳期使用阿兹夫定片和莫诺拉韦胶囊。
(四)孕期住院会诊、转诊与处理
新冠病毒感染孕妇住院期间,产科情况根据产科原则进行处理,但同时也需要关注新冠病毒感染病情,警惕病情进展,及时发现心肺功能异常、生命体征不稳定等情况[28-29]。对于重型和危重型新冠病毒感染孕产妇,在多学科团队指导下选择妊娠期或哺乳期相对安全的药物进行治疗。不具备高危孕产妇及早产儿抢救能力,或患者病情不稳定、重症或危重症患者,接诊医疗机构无重症监护及多学科会诊条件,可以根据当地政策转诊至有救治能力的危重孕产妇和新生儿救治中心。
五、住院分娩
(一)分娩方式的选择
对于重型及危重型新冠病毒感染孕产妇,应由多学科救治团队共同决定分娩时机与分娩方式,重点评估孕妇新冠病毒感染的分型、病程持续时间、严重程度及危险因素。
分娩时机取决于孕妇状态、并发症、孕周、胎儿情况和当地的救治能力。轻型孕妇,如条件允许,对存在终止妊娠指征者,可在感染康复后进行。对出现难治性低氧血症、呼吸衰竭或病情恶化的危重型孕妇,分娩时机需要仔细权衡孕妇和胎儿的获益与风险,需要产科、儿科、母胎医学及重症监护团队的充分沟通[30]。
(二)产时和产后2 h的特殊处理
第一产程应关注生命体征,尤其重视血压、血氧监测,动态评估发展为重型和危重型的风险,注意孕产妇的情绪和心理支持,条件允许时可以有家人陪伴。第二产程,反复的用力呼吸及大便失禁会增加病毒传播风险,建议加强医务人员的个人防护。第三产程,需要预防产后出血。产后需要及时进行血栓风险评估,必要时给予抗凝治疗。重型和危重型患者往往存在凝血功能紊乱,静脉血栓栓塞症风险增加,甚至出现肺栓塞和猝死。根据产妇病情,个体化决定是否抗凝[31]。无症状和轻型产妇,若无其他血栓形成危险因素,无需抗凝治疗;重型及危重型产妇,若无抗凝治疗禁忌证,建议使用预防剂量的抗凝药物;若不存在其他血栓风险,出院后可停用抗凝治疗。
(三)剖宫产术中的麻醉与镇痛
新冠病毒感染不是椎管内麻醉与分娩镇痛的禁忌证,分娩镇痛通过缓解疼痛,达到降低氧耗和心肺功能负担的目的。分娩疼痛会增加产妇潮气量,镇痛可减轻因疼痛和焦虑造成的过度通气,降低病毒传播风险。无论采用分娩镇痛技术阴道分娩或剖宫产,在无椎管内麻醉禁忌证或产科禁忌证时,均以椎管内麻醉或镇痛为首选。应对患者状况进行全面评估,除了呼吸、循环系统和肝肾功能评估之外,尤其需要注意凝血功能。
对存在椎管内麻醉禁忌证、情况紧急或重症感染无法维持充足的氧合时,则应选择全身麻醉。依照孕妇病情需要,术前放置中心静脉导管及桡动脉导管,术中严密监测循环、呼吸、麻醉深度和尿量等。建议采用保护性肺通气策略,并加用呼气末正压通气或间断进行手法肺复张预防术中肺不张;气管拔管期间可给予利多卡因、瑞芬太尼或右美托咪定以避免呛咳;气管拔管时可口鼻覆盖湿纱布以减少分泌物喷出。无论使用何种麻醉方式均应注意监测血氧饱和度及维持血压稳定[32]。
六、新生儿处理
(一)喂养
母乳是婴儿的最佳食物,母乳本身不会传播新冠病毒,应鼓励和支持产妇进行母乳喂养[22,33]。如果母婴同室,母亲在母乳喂养前需做好个人防护,包括佩戴口罩、洗手、清洁乳房等。如果母婴分离,可将母乳挤出后由照护者喂养。产妇应掌握母婴分离时保持泌乳的方法;挤奶前做好洗手、清洁乳房等个人卫生;挤奶后对吸奶器进行必要的清洁消毒。
(二)母婴同室
新冠病毒感染期间母亲产后焦虑和抑郁的发生率增加,长时间的母婴分离对母婴均会带来不利影响。应尽量减少不必要的母婴分离,在做好防护措施的基础上允许母婴接触[34-35],促进母婴互动和依恋关系的建立。
新冠病毒感染孕妇分娩后,应由新生儿医师对新生儿进行及时的健康评估。如一般情况良好而母亲症状明显,可建议暂时母婴分离;新生儿一般情况良好且母亲情况稳定,可母婴同室观察,产妇及陪护者需佩戴N95口罩,做好健康宣教[36]。
(三)感染新生儿的处理要点
分娩时新生儿脐带延迟结扎,及时清洁新生儿,同时进行新冠病毒感染的评估[37]。新生儿出生24 h内呼吸道标本易受母亲羊水及阴道分泌物污染,如需进行核酸或抗原检测,可根据情况选择在生后24~72 h进行首次核酸/抗原检测。新生儿接触新冠病毒感染照护者,如有发热、喂养不耐受、鼻塞、流涕、咳嗽、气促、呕吐、腹泻等临床表现,应进行核酸检测,确定是否为新冠病毒感染,可考虑转入新生儿病区治疗。
目前暂不推荐新生儿接种新冠病毒疫苗。
七、产褥期保健
产妇合并新冠病毒感染时,产科情况恢复良好的轻型或无症状者体温正常超过24 h即可出院。如有肺部影像学异常,则在其急性渗出性病变明显改善,无其他并发症时考虑出院[38]。
出院后,除常规产科随访外,需要注意其是否存在发展为重型感染的高危因素,如产后出血、疲劳、妊娠期贫血、伴有肥胖和高血压等基础疾病等。需要注意有无新发呼吸困难或加重,注意头晕、意识模糊等神志改变,必要时需要监测血氧情况。提供相关知识的宣教,建议产妇充分的休息、足够的营养和进行必要的监测等。
产褥期发热需要及时进行新冠病毒感染的筛查和诊断[39],需要与常见的产褥期感染进行鉴别,如子宫内膜炎、手术部位感染、乳腺炎、流行性呼吸道感染、肾盂肾炎、其他病毒性或细菌性呼吸道感染等。结合症状、体格和实验室检查结果通常可以区分这些疾病。但也要注意两者可能并存的情况。
八、心理指导与支持
作为生理和心理处于特殊时期的人群,新冠病毒感染的孕产妇心理问题可能会增加,主要表现为失眠、焦虑(包括惊恐发作)、抑郁、疑病、强迫等。应规范开展孕产妇心理症状的筛查和干预。对于既往有抑郁或焦虑病史、有心理疾病家族史等高危人群,产科医师可以联合心理科医师在线上、线下给予孕期教育,介绍孕期相关知识、不同孕周检查内容以及分娩时注意事项等。
按照具体情况,及时在心理专科门诊、产科门诊进行多学科分层分级诊治。轻度心理障碍的孕产妇,妇产科联合心理专科医师及时给予非药物干预。中、重度心理障碍的孕产妇,可以在专科病房与专科医院住院处置,启动多学科团队心理诊治模式,给予非药物干预和/或药物干预综合治疗,药物干预参考妊娠期精神科药物分级并遵循个体化原则[40]。
利益冲突 所有作者声明无利益冲突
参考文献 [1] 中华人民共和国卫生健康委员会.新型冠状病毒感染诊疗方案(试行第九版)[OL].(2022-03-15)[2023-01-30]. http://www.gov.cn/zhengce/zhengceku/2022-03/15/5679257/files/49854a49c 7004f4ea9e622f3f2c568d8.pdf. National Health Commission of the People's Republic of China. Diagnosis and Treatment Protocol for COVID-19 (Trial 9th version)[OL].(2022-03-15)[2023-01-30]. http://www.gov.cn/zhengce/zhengceku/2022-03/15/5679257/files/49854a49c7004f4e a9e622f3f2c568d8.pdf. [2] Yang R, Mei H, Zheng T, et al. Pregnant women with COVID-19 and risk of adverse birth outcomes and maternal-fetal vertical transmission: a population-based cohort study in Wuhan, China[J]. BMC Med, 2020,18(1):330. DOI: 10.1186/s12916-020-01798-1. [3] Zambrano LD, Ellington S, Strid P, et al. Update: characteristics of symptomatic women of reproductive age with laboratory-confirmed SARS-CoV-2 infection by pregnancy status - United States, January 22-October 3, 2020[J]. MMWR Morb Mortal Wkly Rep, 2020,69(44):1641-1647. DOI: 10.15585/mmwr.mm6944e3. [4] Lokken EM, Huebner EM, Taylor GG, et al. Disease severity, pregnancy outcomes, and maternal deaths among pregnant patients with severe acute respiratory syndrome coronavirus 2 infection in Washington State[J]. Am J Obstet Gynecol, 2021,225(1):77.e1-77.e14. DOI: 10.1016/j.ajog.2020.12.1221. [5] Juan J, Gil MM, Rong Z, et al. Effect of coronavirus disease 2019 (COVID-19) on maternal, perinatal and neonatal outcome: systematic review[J]. Ultrasound Obstet Gynecol, 2020,56(1):15-27. DOI: 10.1002/uog.22088. [6] Gracia-Perez-Bonfils A, Martinez-Perez O, Llurba E, et al. Fetal heart rate changes on the cardiotocograph trace secondary to maternal COVID-19 infection[J]. Eur J Obstet Gynecol Reprod Biol, 2020,252:286-293. DOI: 10.1016/j.ejogrb.2020.06.049. [7] Pineles BL, Stephens A, Narendran LM, et al. The relationship between delivery and the PaO2 /FiO2 ratio in COVID-19: a cohort study[J]. BJOG, 2022,129(3):493-499. DOI: 10.1111/1471-0528.16858. [8] Metz TD, Clifton RG, Hughes BL, et al. Disease severity and perinatal outcomes of pregnant patients with coronavirus disease 2019 (COVID-19)[J]. Obstet Gynecol, 2021,137(4):571-580. DOI: 10.1097/AOG.0000000000004339. [9] Pierce-Williams R, Burd J, Felder L, et al. Clinical course of severe and critical coronavirus disease 2019 in hospitalized pregnancies: a United States cohort study[J]. Am J Obstet Gynecol MFM, 2020,2(3):100134. DOI: 10.1016/j.ajogmf.2020. 100134. [10] DeSisto CL, Wallace B, Simeone RM, et al. Risk for stillbirth among women with and without COVID-19 at delivery hospitalization - United States, March 2020-September 2021[J]. MMWR Morb Mortal Wkly Rep, 2021,70(47):1640-1645. DOI: 10.15585/mmwr.mm7047e1. [11] Conde-Agudelo A, Romero R. SARS-CoV-2 infection during pregnancy and risk of preeclampsia: a systematic review and meta-analysis[J]. Am J Obstet Gynecol, 2022,226(1):68-89.e3. DOI: 10.1016/j.ajog.2021.07.009. [12] Chmielewska B, Barratt I, Townsend R, et al. Effects of the COVID-19 pandemic on maternal and perinatal outcomes: a systematic review and meta-analysis[J]. Lancet Glob Health, 2021,9(6):e759-e772. DOI: 10.1016/S2214-109X(21)00079-6. [13] 中华人民共和国卫生健康委员会.新型冠状病毒感染重症病例诊疗方案 (试行第四版)[S/OL].(2023-01-13)[2023-01-30].http://www.nhc.gov.cn/ylyjs/pqt/202301/ad34a9b598654b90a5c8c99440cce21b/files/754297ec20cd40eebb7fe18828d8ed31.pdf. National Health Commission of the People's Republic of China. Diagnosis and Treatment Protocol for Severe Cases of COVID-19 (Trial 4th Version) [OL].(2023-01-13)[2023-01-30].http://www.nhc.gov.cn/ylyjs/pqt/202301/ad34a9b598654b90a5c8c99440cce21b/files/754297ec20cd40eebb7fe18828d8ed31.pdf. [14] Mihajlovic S, Nikolic D, Santric-Milicevic M, et al. Four waves of the COVID-19 pandemic: comparison of clinical and pregnancy outcomes[J]. Viruses, 2022,14(12):2648.DOI: 10. 3390/v14122648. [15] Nana M, Hodson K, Lucas N, et al. Diagnosis and management of covid-19 in pregnancy[J]. BMJ, 2022,377:e069739. DOI: 10.1136/bmj-2021-069739. [16] Aabakke A, Petersen TG, Wøjdemann K, et al. Risk factors for and pregnancy outcomes after SARS-CoV-2 in pregnancy according to disease severity: A nationwide cohort study with validation of the SARS-CoV-2 diagnosis[J]. Acta Obstet Gynecol Scand, 2023,102(3):282-293. DOI: 10.1111/aogs.14512. [17] Wang C, Chen DJ, Yang HX. Updates on COVID-19 infection during pregnancy[J]. Matern Fetal Med, 2020,2(2):65-67. DOI: 10.1097/FM9.0000000000000049. [18] Yan J, Guo J, Fan C, et al. Coronavirus disease 2019 in pregnant women: a report based on 116 cases[J]. Am J Obstet Gynecol, 2020,223(1):111.e1-111.e14. DOI: 10.1016/j.ajog.2020.04.014. [19] Jamieson DJ, Rasmussen SA. An update on COVID-19 and pregnancy[J]. Am J Obstet Gynecol, 2022,226(2):177-186. DOI: 10.1016/j.ajog.2021.08.054. [20] Smith ER, Oakley E, Grandner GW, et al. Clinical risk factors of adverse outcomes among women with COVID-19 in the pregnancy and postpartum period: a sequential, prospective meta-analysis[J]. Am J Obstet Gynecol, 2023,228(2):161-177. DOI: 10.1016/j.ajog.2022.08.038. [21] World Health Organization. Definition and categorization of the timing of mother-to-child transmission of SARS-CoV-2[OL].(2020-02-07)[2023-01-30].https://www.who.int/publications/i/item/WHO-2019-nCoV-mother-to-child-transmission-2021.1. [22] Chen H, Guo J, Wang C, et al. Clinical characteristics and intrauterine vertical transmission potential of COVID-19 infection in nine pregnant women: a retrospective review of medical records[J]. Lancet, 2020,395(10226):809-815. DOI: 10.1016/S0140-6736(20)30360-3. [23] Fenizia C, Saulle I, Di Giminiani M, et al. Unlikely SARS-CoV-2 transmission during vaginal delivery[J]. Reprod Sci, 2021,28(10):2939-2941. DOI: 10.1007/s43032-021-00681-5. [24] Drugs.com[EB]. https://www.drugs.com/drug_information.html. [25] Hale TW. Medication and mothers' milk[M]. 18th ed. New York: Springer Publishing Com., 2019:3-451. [26] Briggs G. Drugs in pregnancy and lactation: A reference guide to fetal and neonatal risk[M]. 12th ed. Washington: Lippincott Williams & Wilkins (LWW), 2019:71-3286. [27] 中华人民共和国卫生健康委员会.新型冠状病毒感染诊疗方案(试行第十版)[S/OL].(2023-01-06)[2023-01-30]. http://www.nhc.gov.cn/xcs/zhengcwj/202301/32de5b2ff9bf4eaa88e75bdf722 3a65a/files/02ec13aadff048ffae227593a6363ee8.pdf. National Health Commission of the People's Republic of China. Diagnosis and treatment protocol for COVID-19 (Trial 10th version) [OL].(2023-01-06)[2023-01-30]. http://www.nhc.gov.cn/xcs/zhengcwj/202301/32de5b2ff9bf4eaa88e75bdf7223a65a/files/02ec13aadff048ffae227593a6363ee8.pdf. [28] Sokou R, Konstantinidi A, Boutsikou T, et al. Breastfeeding in the era of COVID-19. A narrative review[J]. J Obstet Gynaecol, 2022,42(4):539-545. DOI: 10.1080/01443615.2021.1929112. [29] Chambers C, Krogstad P, Bertrand K, et al. Evaluation for SARS-CoV-2 in breast milk from 18 infected women[J]. JAMA, 2020,324(13):1347-1348. DOI: 10.1001/jama.2020. 15580. [30] Slayton-Milam S, Sheffels S, Chan D, et al. Induction of labor in an intubated patient with coronavirus disease 2019 (COVID-19)[J]. Obstet Gynecol, 2020,136(5):962-964. DOI: 10.1097/AOG. 0000000000004044. [31] Metz TD, Clifton RG, Hughes BL, et al. Association of SARS-CoV-2 infection with serious maternal morbidity and mortality from obstetric complications[J]. JAMA, 2022,327(8):748-759. DOI: 10.1001/jama.2022.1190. [32] Bajwa S, Sharma R, Kurdi MS, et al. Anesthesia management in a post Covid-19 obstetric patient-What we need to know[J]. J Anaesthesiol Clin Pharmacol, 2022,38(Suppl 1):S13-S21. DOI: 10.4103/joacp.joacp_550_21. [33] Qiao J. What are the risks of COVID-19 infection in pregnant women?[J]. Lancet, 2020,395(10226):760-762. DOI: 10.1016/S0140-6736(20)30365-2. [34] American Academy of Pediatrics Initial Guidance. Management of infants born to mothers with COVID-19[OL].(2020-06-28)[2023-01-30]. https://downloads.aap.org/AAP/PDF/COVID%2019%20Initial%20Newborn%20Guidance.pdf. [35] Kest H, Kaushik A, Skroce L, et al. Rooming-in for well-term infants born to asymptomatic mothers with COVID-19: correspondence[J]. J Pediatric Infect Dis Soc, 2021,10(1):60-61. DOI: 10.1093/jpids/piaa120. [36] 王晨,杨慧霞.重视新型冠状病毒感染对母婴的影响[J].中华妇产科杂志,2020,55(3):147-149.DOI:10.3760/cma.j.cn112141- 20200229-00151. Wang C, Yang HX. Attach importance to COVID-19 infection on maternal and infant outcomes[J].Chin J Obstet Gynecol,2020,55(3):147-149.DOI:10.3760/cma.j.cn112141-20200229-00151. [37] Shahbazi Sighaldeh S, Ebrahimi Kalan M. Care of newborns born to mothers with COVID-19 infection; a review of existing evidence[J]. J Matern Fetal Neonatal Med, 2022,35(11):2203-2215. DOI: 10.1080/14767058.2020.1777969. [38] American College of Obstetricians and Gynecologists. COVID-19 FAQs for Obstetrician-Gynecologists, Obstetrics[J/OL].(2022-09-20)[2023-01-30].https://www.acog.org/clinical- information/physician-faqs/covid-19-faqs-for-ob-gyns-obstetrics. [39] Hirshberg JS, Stout MJ, Raghuraman N. Coronavirus disease 2019 infection among asymptomatic and symptomatic pregnant women: two weeks of confirmed presentations to an affiliated pair of New York City hospitals[J]. Am J Obstet Gynecol MFM, 2020,2(3):100162. DOI: 10.1016/j.ajogmf.2020.100162. [40] Gimbel LA, Allshouse AA, Neff D, et al. Mental health symptom changes in pregnant individuals across the COVID-19 pandemic: a prospective longitudinal study[J]. BMC Pregnancy Childbirth, 2022,22(1):897. DOI: 10.1186/s12884-022-05144-6. 本文引用格式:陈敦金,戴月,刘兴会,等. 孕产妇合并新型冠状病毒感染诊治推荐意见[J]. 中华围产医学杂志, 2023, 26(6): 441-447. DOI: 10.3760/cma.j.cn113903-20230130-00042. 本文首次发表在Maternal-Fetal Medicine, 2023,5(2):74-79. DOI:10.1097/FM9.0000000000000186. 来源:中华围产医学杂志 作者:陈敦金1 戴月2 刘兴会3 漆洪波4 王晨5 王岚4 魏瑗6 徐晓超2 张川3 张伶俐3 张玉泉7 赵瑞华8赵扬玉6 周伯荣1 王爱玲9 杨慧霞5 宋莉2 单位:1. 广州医科大学附属第三医院妇产科;2. 国家卫生健康委员会妇幼健康司;3. 四川大学华西第二医院妇产科;4. 重庆市妇幼保健院行政办公室;5. 北京大学第一医院妇产科(妊娠合并糖尿病母胎医学北京市重点实验室);6. 北京大学第三医院妇产科;7. 南通大学附属医院妇产科;8. 中国中医科学院广安门医院妇产科;9. 中国疾病预防控制中心妇幼保健中心
