中华医学会
地址: 中国北京东四西大街42号
邮编: 100710
支气管肺发育不良与早产儿视网膜病变的围产期影响因素及可能关系
本文引用格式:李亚男, 江倩男, 吕朦, 等. 支气管肺发育不良与早产儿视网膜病变的围产期影响因素及可能关系[J]. 中华围产医学杂志, 2024, 27(2): 111-117. DOI: 10.3760/cma.j.cn113903-20230824-00154.
摘要
目的 探讨支气管肺发育不良(bronchopulmonary dysplasia,BPD)与早产儿视网膜病变(retinopathy of prematurity,ROP)的围产期危险因素及相关性。
方法 回顾性分析2017年6月至2022年7月于青岛大学附属妇女儿童医院新生儿重症监护病房住院的173例胎龄<32周的BPD早产儿的病例资料,根据是否发生ROP分为ROP组(n=64)和非ROP组(n=109)。采用χ2检验、两独立样本t检验和Mann-Whitney U检验比较组间一般资料、治疗及并发症的发生情况,采用多因素logistic逐步回归分析BPD早产儿发生ROP的独立危险因素,并利用受试者工作特征(receiver operating characteristic,ROC)曲线评估危险因素预测BPD早产儿发生ROP的价值。同时分析BPD严重程度与ROP发病的关系。
结果 ROP组患儿的出生胎龄[(28.0±1.1)与(28.8±1.2)周,t=4.01]、出生体重[(1 075.9±141.4)与(1 143.2±168.6) g,t=2.68]、动脉血二氧化碳分压[42.5 mmHg(1 mmHg=0.133 kPa)(34.0~51.0 mmHg)与47.0 mmHg(39.0~54.0 mmHg),Z=-2.31]和第1天液体入量[80.0 ml(72.3~88.7 ml)与83.6 ml(76.6~92.8 ml),Z=-2.28]均低于非ROP组,凝血酶原时间[15.7 s(14.1~17.7 s)与14.6 s(13.1~16.7 s),Z=-2.17]、活化部分凝血活酶时间[64.7 s(52.9~77.9 s)与55.8 s(48.4~68.9 s),Z=-2.12]、应用肺表面活性物质的比例[71.9%(46/64)与49.5%(54/109),χ2=8.25]、总用氧时间[50.5 d(40.0~64.0 d)与45.0 d(37.0~52.0 d),Z=-2.77]、有创通气时间[5.0 d(1.0~11.0 d)与1.0 d(0.0~5.0 d),Z=-4.03]、无创通气或高流量氧疗时间[(31.7±12.7)与(26.4±13.1) d,t=-2.59]、新生儿呼吸窘迫综合征发生率[76.6%(49/64)与57.8%(63/109),χ2=6.22]均较非ROP组增加(P值均<0.05)。ROP组与非ROP组间使用激素治疗BPD的比例差异无统计学意义[60.3%(38/63)与74.3%(81/109),χ2=3.67,P=0.055]。多因素logistic逐步回归分析发现,胎龄小(OR=1.599,95%CI:1.126~2.272,P=0.009)、第1天液体入量少(OR=1.033,95%CI:1.004~1.062,P=0.024)、有创通气时间长(OR=1.076,95%CI:1.017~1.138,P=0.011)是BPD患儿发生ROP的独立危险因素,应用激素治疗BPD是BPD患儿发生ROP的独立保护因素(OR=0.378,95%CI:0.173~0.827,P=0.015)。轻、中度BPD患儿中,非ROP患儿的比例较大,分别为64.6%(73/113)和66.7%(34/51),而重度BPD患儿中合并ROP的比例较大(7/9)(χ2=6.84,P=0.033)。
结论 胎龄小、有创通气时间长、第1天液体入量少的BPD患儿更易发生ROP,而应用激素治疗的BPD患儿较不容易发生ROP。重度BPD可能增加患儿发生ROP的风险。
【关键词】 支气管肺发育不良;早产儿视网膜病变;危险因素
支气管肺发育不良(bronchopulmonary dysplasia,BPD)和早产儿视网膜病变(retinopathy of prematurity,ROP)均是与吸氧及异常血管发育相关的早产儿后遗症。随着国内早产儿救治技术的进步,极早产儿存活率不断提高,BPD及ROP发生率也随之增加。BPD是各种因素引起的肺泡及肺血管发育障碍,是极早产儿最常见的慢性肺部疾病之一。ROP是早产儿眼部并发症之一,与视网膜新生血管形成相关,可引起牵引性视网膜脱离及失明,是婴幼儿致盲及致低视力眼病中最为多见的疾病。据估计,60%~71%的BPD早产儿合并ROP,表明这2种疾病之间存在潜在的关联[1]。ROP的发病与BPD的许多治疗措施,如吸氧、机械通气等有关[2]。高氧会激活促炎细胞因子,导致血管生长受阻,从而导致视网膜缺氧,触发异常血管生成,是视网膜炎症的重要驱动因素[3]。目前有关BPD与ROP相关性的临床研究甚少,故本研究旨在探讨BPD与ROP的危险因素及相关性,为BPD及ROP的预防及精细化治疗提供参考。
资料与方法
一、研究对象
本研究为回顾性病例对照研究。
1.纳入标准:(1)2017年6月至2022年7月于青岛大学附属妇女儿童医院新生儿重症监护病房住院;(2)出生胎龄
2.排除标准:(1)放弃治疗或病历资料不完整;(2)合并严重先天畸形、复杂性先天性心脏病、遗传代谢性疾病等;(3)住院期间有严重合并症,如严重窒息、败血症并多脏器衰竭、严重脑积水或脑室周围白质软化等,或因新生儿坏死性小肠结肠炎、颅内出血等行外科手术治疗者。
研究期间符合纳入标准者293例,排除放弃治疗17例,资料不完整23例,严重先天畸形、复杂性先天性心脏病、遗传代谢性疾病、严重合并症、因其他疾病行外科手术治疗等80例,最终173例纳入分析。本研究经青岛大学附属妇女儿童医院医学伦理委员会批准(QFELL-YJ-2022-58)。
二、研究方法
1.资料收集:通过病历信息系统收集患儿临床资料。(1)一般资料:胎龄、出生体重、性别、娩出方式、是否为多胎等。(2)母亲资料:妊娠期是否有胎膜早破、胎盘早剥及产前是否促胎肺成熟等。(3)并发症及治疗情况:是否合并动脉导管未闭、≥Ⅱ期新生儿坏死性小肠结肠炎等并发症;住院期间总用氧时间、不同通气方式用氧时间、是否应用肺表面活性物质、是否应用激素治疗BPD、生后第1天液体入量(液体摄入总量)、生后第1次动脉血气[pH值、动脉血氧分压(arterial partial pressure of oxygen,PaO2)、动脉血二氧化碳分压(partial pressure of carbon dioxide,PaCO2)]及凝血常规等指标。
2.相关诊断标准:(1)BPD:根据2001年美国国立儿童健康与人类发育研究所提出的BPD诊断标准[4],即任何氧依赖[吸入氧浓度(fraction of inspired oxygen,FiO2)>21%]超过28 d的新生儿。胎龄<32周者,根据校正胎龄36周或出院时是否需要氧气,将BPD分为轻度(未使用氧气)、中度(FiO2<30%)和重度(FiO2≥30%或需要正压通气或经鼻持续气道正压通气以及机械通气)。(2)ROP:根据“中国早产儿视网膜病变分类和治疗专家共识(2023年)”[5]进行复核诊断。(3)高氧血症:PaO2>100 mmHg(1 mmHg= 0.133 kPa)[6]。
3.分组及分析:根据患儿是否发生ROP分为ROP组(n=64)和非ROP组(n=109)。比较组间临床情况的差异,分析BPD早产儿发生ROP的危险因素及BPD与ROP的相关性。
三、统计学分析
应用SPSS 26.0统计软件进行数据分析。计数资料采用频数及率表示,组间比较采用χ2检验;符合正态分布的计量资料以±s表示,组间比较采用两独立样本t检验;非正态分布的计量资料用M(P25~P75)表示,组间比较采用Mann-Whitney U检验。采用χ2检验分析BPD严重程度与ROP发病的相关性。BPD患儿发生ROP的危险因素分析采用多因素logistic逐步回归分析。采用受试者工作特征(receiver operating characteristic, ROC)曲线分析危险因素预测ROP的价值。P<0.05为差异有统计学意义。
结果
173例BPD患儿中男95例,女78例;胎龄为(28.5±1.3)周(25.6~31.6周),出生体重为(1 118.3± 162.0) g(700~1 600 g),其中胎龄≤27+6、28+0~29+6、30+0~31周+6分别为67、89和17例;BPD轻、中、重度分别为113、51和9例。
一、BPD患儿发生ROP的危险因素的单因素分析
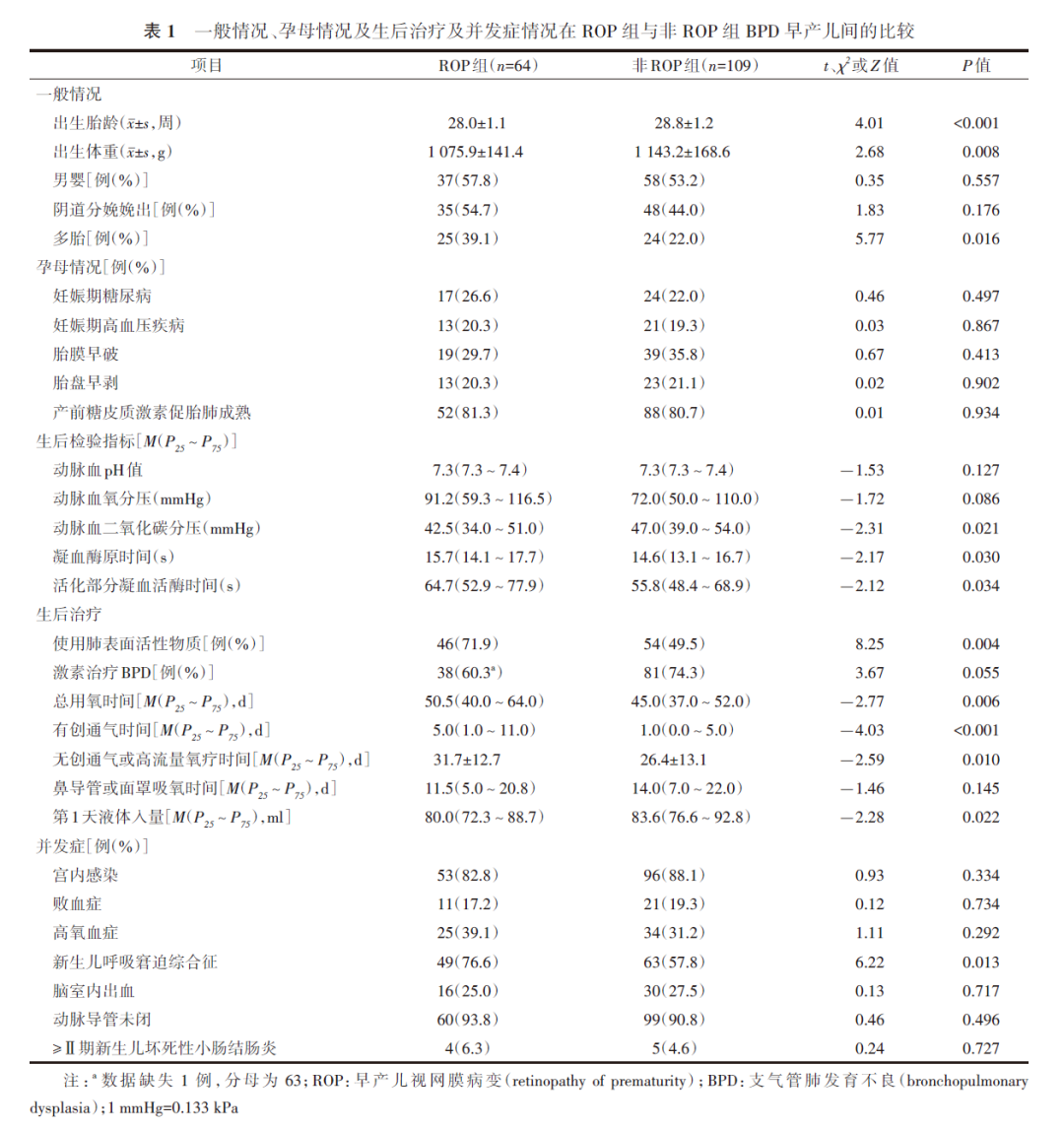
1. 2组一般资料及孕母情况比较:与非ROP组相比,ROP组早产儿出生胎龄和出生体重更低、多胎比例更高(P值均<0.05)。2组患儿的娩出方式、性别构成以及母亲妊娠期高血压疾病、妊娠期糖尿病、胎膜早破、胎盘早剥及产前糖皮质激素促胎肺成熟的比例差异均无统计学意义(P值均>0.05)。见表1。
2. 2组患儿生后检验指标、治疗及并发症情况比较:与非ROP组相比,ROP组患儿PaCO2更低,第1天液体入量更少,凝血酶原时间、活化部分凝血活酶时间、使用肺表面活性物质比例、总用氧时间、有创通气时间、无创通气或高流量氧疗时间以及新生儿呼吸窘迫综合征发生率增加(P值均<0.05)。见表1。
二、BPD患儿发生ROP危险因素的多因素分析
将应用激素治疗BPD及表1中差异有统计学意义的因素纳入多因素logistic逐步回归分析,结果表明胎龄小(OR=1.599,95%CI:1.126~2.272,P=0.009)、第1天液体入量少(OR=1.033,95%CI:1.004~1.062,P=0.024)、有创通气时间长(OR=1.076,95%CI:1.017~1.138,P=0.011)是BPD患儿发生ROP的独立危险因素,应用激素治疗BPD是BPD早产儿发生ROP的独立保护因素(OR=0.378,95%CI:0.173~0.827,P=0.015)。
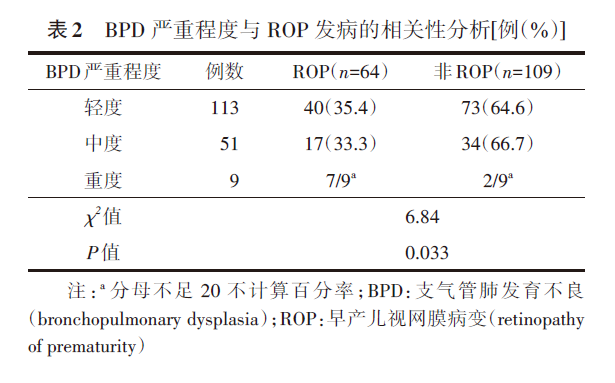
三、BPD严重程度与ROP发病的相关性分析
轻、中度BPD患儿中,非ROP比例较大,而重度BPD患儿中合并ROP的比例较大(P=0.033)。见表2。
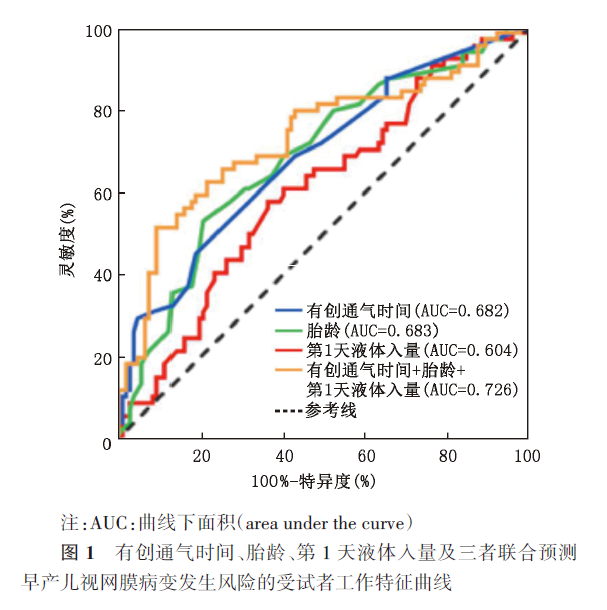
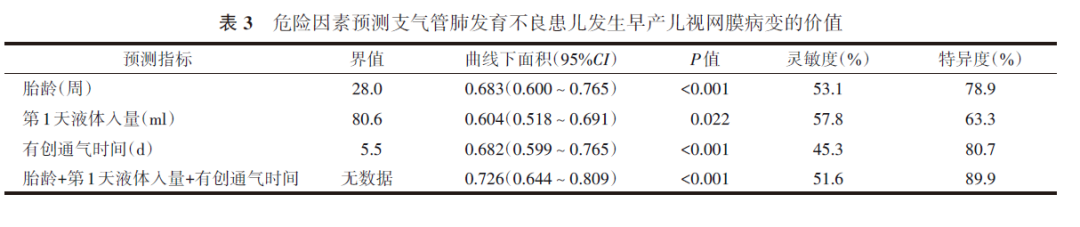
四、危险因素对BPD患儿发生ROP的预测价值
绘制胎龄、第1天液体入量、有创通气时间及三者联合预测BPD患儿发生ROP风险的ROC曲线,结果显示三者联合预测BPD患儿发生ROP的特异度最高,但灵敏度只有51.6%。见图1和表3。
讨论
一、胎龄和出生体重对BPD和ROP的影响
BPD和ROP均是多种因素共同作用的疾病,预防和临床管理需考虑各种因素。研究表明,胎龄越小、出生体重越低的早产儿,BPD和ROP的发生率越高[2]。本研究ROP组患儿胎龄、出生体重较小,且胎龄小为ROP的独立危险因素,ROC曲线分析提示胎龄界值为28.0周时预测ROP的特异度较高(78.9%)。视网膜的血管发育始于视神经乳头,在血管内皮生长因子的影响下,从中心到周围形成新的血管。视网膜血管发育成熟发生在校正胎龄40~44周,早产可导致视网膜血管发育过程中断[7]。早产儿各器官系统发育不完善,胎龄越小,呼吸中枢和肺部的发育程度也越低,导致BPD的发生风险增加,严重程度加剧。因此,强化围产期的保健措施,降低早产率,是预防BPD和ROP的重要举措。
二、用氧与BPD和ROP
早产儿对氧气极为敏感,容易发生氧损伤。吸入高浓度氧气会直接伤害肺泡上皮细胞和毛细血管内皮细胞,导致肺泡毛细血管通透性增加,从而加重肺泡渗出。长时间通气可能引发一系列炎症反应,并产生炎症介质,最终导致肺部受损。高浓度氧气可以导致视网膜血管收缩,引发视网膜缺氧,并刺激血管生成因子的产生,从而促进新生血管的形成,增加了发生ROP的风险。长时间高浓度吸氧是BPD和ROP的重要诱因,但关于吸氧浓度及持续时间的影响研究结果并不一致。Sharma等[8]的研究结果表明早产儿生后第1天最大FiO2>40%可预测中/重度BPD的发生,而动物实验证明,FiO2>85%并持续10~14 d可导致小鼠发生BPD[9-10],暴露于75%的氧气中5 d不但导致小鼠ROP,同时也会产生与BPD类似的肺部损伤[11]。本研究结果显示,ROP组有创通气、无创通气或高流量氧疗时间较长,有创通气时间长为<32周BPD早产儿发生ROP的独立危险因素,与Podraza等[12]的研究结果相似。避免机械通气时间>14 d可能会将早产儿BPD的发生风险降低18%,严重ROP的风险降低14%[13]。
早产儿抗氧化能力差,易出现高氧损伤,根据“早产儿治疗用氧和视网膜病变防治指南(修订版)”[14],早产儿治疗用氧的理想目标是维持PaO2在50~80 mmHg。本研究中,ROP组高氧血症患儿的比例为39.1%(25/64),并不高于非ROP组[31.2%(34/109)](χ2=1.11,P=0.292),考虑原因是本研究统计的是生后第1次的血气分析结果,且没有分析高氧血症的持续时间,样本量也有限。
维持适当的血氧饱和度一直是预防BPD和ROP的主要手段之一。Meta分析显示,低血氧饱和度组(85%~89%)患儿的病死率增加,而高血氧饱和度组(91%~95%)患儿ROP发生率增加[15]。ROP的发展可以分为2个阶段:第一阶段是视网膜血管的阻塞或发育受阻;第二阶段是视网膜缺氧引起的病理性血管生长和新生血管形成。研究表明,在复苏期间和校正胎龄30~32周,高氧可以增加ROP的患病风险;而校正胎龄>32周时,缺氧可增加ROP的患病风险。回顾性队列研究认为,根据不同阶段调整目标血氧饱和度可以减少ROP的发生[16]。
三、液体量与BPD和ROP
本研究统计了早产儿生后第1天的液体入量,单因素及多因素分析结果均显示第1天液体入量少是BPD早产儿发生ROP的危险因素。在极低出生体重儿的临床管理中,液体平衡与BPD的相关性一直存在争议。有研究表明极低出生体重儿早期液体超负荷与较高的病死率、较高的平均气道压以及生后最初7 d较长的机械通气持续时间有关[17]。一项单中心回顾性研究认为中重度BPD患儿的平均液体摄入量更高[18]。临床上多通过限制BPD高危儿液体入量,以预防肺水肿及有血流动力学影响的动脉导管未闭的发生,理想情况下,BPD早产儿应接受不超过135~150 ml/(kg·d)的液体摄入[19]。然而过度限制液体入量会导致热量供给不足和营养素摄入不足,对肺部的生长和修复过程不利,促进BPD的发展[20-21],能量及营养素摄入不足也会影响ROP的进展[22]。有研究建议极低出生体重儿生后第1天液体入量为70~80 ml/kg,逐步从肠外营养过渡到肠内喂养[23]。对极低出生体重儿的液体平衡的管理仍有待进一步研究。
四、感染/炎症与BPD和ROP
感染/炎症反应在BPD和ROP的发病过程中扮演着重要角色。高氧是视网膜炎症的重要驱动因素,可激活小胶质细胞产生白细胞介素-1β等促炎细胞因子分泌,导致血管生长受阻,远端视网膜缺氧,从而引发异常的血管生成[24]。本研究中,ROP组败血症患儿为11例(17.2%),非ROP组为21例(19.3%),2组间差异无统计学意义(χ2=0.12,P=0.734),与目前研究得出的早产儿败血症是BPD和ROP的重要危险因素[25-26]的结果不一致,考虑原因可能是干扰因素较多影响单因素分析的结果,需进一步扩大样本量的深入研究。
糖皮质激素具有抗炎和降低毛细血管通透性的作用,生后应用已被证明可以降低BPD的发生率,但因其神经系统副作用,在BPD的预防应用中受到限制[27]。研究表明,糖皮质激素治疗BPD和严重ROP之间存在相关性,特别是在胎龄24~26周的早产儿中,糖皮质激素治疗BPD增加了患严重ROP的风险[28]。但糖皮质激素的使用时间、种类及给药途径在BPD患儿中的应用尚存在争议,用药的疗效及远期预后也需进一步证明[29]。本研究结果显示应用激素治疗BPD是ROP发生的独立保护因素(OR=0.378,P=0.015),与上述研究结果不同,其原因可能与研究群体的选择不同有关。研究发现血液黏稠、PaCO2过低、酸中毒等可能与ROP的发生有一定关系[30],本研究单因素分析显示ROP组早产儿生后第1次PaCO2低,活化部分凝血活酶时间及凝血酶原时间长,但多因素分析并未发现这些因素是ROP的危险因素,可能原因是本研究只统计生后第1次检查的指标,未进行动态观察,未来可以加大样本量并观察患儿相关化验指标的变化趋势,以更全面地了解其与ROP的关系。
五、BPD与ROP的关系
本研究分析了BPD的严重程度对于ROP发生情况的影响,结果显示轻、中度BPD早产儿ROP的发生率小于重度BPD早产儿,在一定程度上表明重度BPD早产儿发生ROP的风险可能增加。
综上所述,本研究发现胎龄、有创通气时间、第1天液体入量及生后激素治疗情况可影响BPD患儿ROP的发生,重度BPD可能增加ROP的发生风险。然而,本研究是单中心研究,结果难免存在偏倚,未来需要进一步扩大样本量、进行多中心研究深入探讨BPD与ROP的关系。
利益冲突 所有作者声明无利益冲突
参考文献略
